中枢神经系统(CNS)疾病治疗长期受困于血脑屏障(BBB)的药物阻碍问题,传统免疫细胞递送策略又因脱靶分布、免疫排斥等缺陷难以突破瓶颈。2026年1月16日,清华大学张明君教授与北京天坛医院王伊龙教授团队在Cell期刊发表研究论文,首次提出利用颅骨骨髓免疫细胞作为药物载体,通过颅骨-脑膜微通道(SMCs)绕过血脑屏障,实现CNS病灶靶向递送,为神经疾病治疗开辟新路径。

研究基于颅骨骨髓与脑膜间特殊通道的生物学特性,开发载药纳米颗粒“劫持”颅骨免疫细胞的技术。该策略通过在颅骨骨髓内原位构建载药细胞,利用其天然趋化能力经SMCs定向迁移至脑内病灶。临床前脑卒中动物模型显示,该方法仅需传统剂量1/15即可显著改善急性期症状及长期预后,且探索性临床研究验证了其安全性与转化潜力。这一突破不仅解决了药物递送效率问题,更揭示了颅骨免疫通路作为微创、高效“生物物料传输通道”的潜力。
清华大学张明君教授、北京天坛医院王伊龙教授为该文章的共同通讯作者,清华大学高喜泽博士、国家神经系统疾病临床医学研究中心刘向荣研究员、北京天坛医院博士生王楠星为共同第一作者。清华大学博士生崔承前、宁艾一,北京天坛医院医生刘伟明、杨沫、欧云尉,北京大学博士生邱硕文、研究员卢萌,西北工业大学副教授孙乐明、博士生雷扬和付董洁对本研究有直接贡献。
研究团队进一步指出,该通路可与脑机接口技术融合,发展为承载“物料流、能量流、信息流”的多方位交互接口。通过微纳机器人实现基于脑神经信号反馈的药物闭环递送,有望打破生物进化保护形成的交互屏障,为脑机智能融合研究提供新思路。
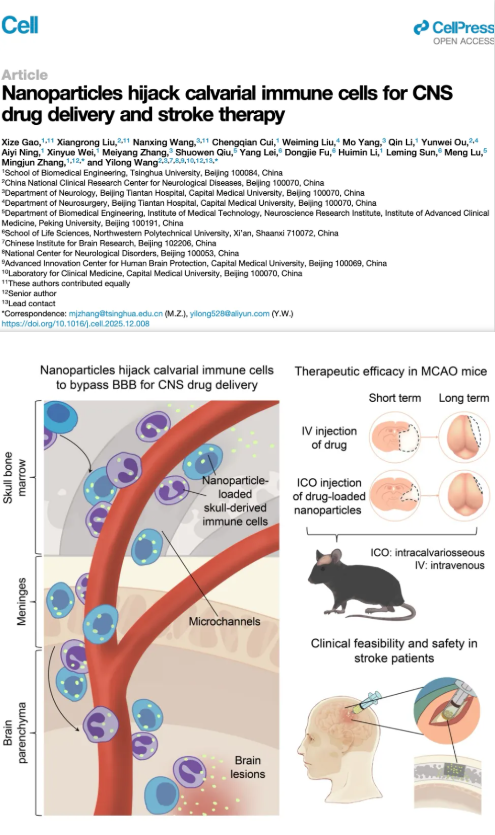
出版详情:标题:《Nanoparticles hijack calvarial immune cells for CNS drug delivery and stroke therapy》,发表于:《Cell期刊》。
