香港科技大学(HKUST)的研究团队在RNA沉默机制领域取得重要进展,揭示了人类DICER酶如何以单核苷酸精度切割microRNAs(miRNAs)。这一发现为基因调控研究提供了新见解,并有助于理解癌症、免疫紊乱和遗传性疾病的分子机制。
该研究由生命科学部副教授Tuan Anh Nguyen领导,博士生Minh Khoa Ngo和Cong Truc Le共同参与,成果已在《自然》杂志发表,论文题为“DICER切割保真度由5′-末端结合口袋调控”。研究团队运用高分辨率冷冻电子显微镜(cryo-EM)和生化技术,在原子层面观察了DICER与RNA的相互作用。
在RNA调控过程中,DICER酶作为“分子剪刀”将双链RNA前体切割成短调控RNA,这些RNA随后被整合到RNA诱导沉默复合物(RISC)中,帮助细胞识别并抑制错误遗传信息。研究人员长期致力于探索DICER实现高精度切割的机制。
第一作者Minh Khoa Ngo表示:“冷冻电子显微镜让我们能够从原子细节上观察RNA底物与DICER的相互作用。这些结构快照揭示了DICER在处理不同RNA序列时的动态调整,重塑了我们对酶功能的理解。”团队发现,DICER在切割前会进行构象调整,引导RNA进入正确位置,并通过5′-末端结合口袋内的氨基酸精确对齐RNA。
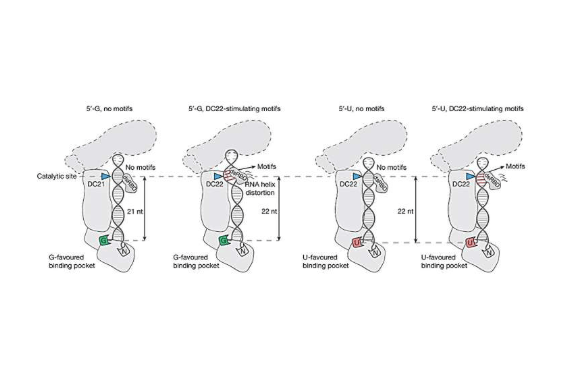
通讯作者Nguyen教授指出:“这类似于剪刀能‘读取’RNA的切割位置,确保信息完整性。研究不仅确认了已知的U偏好5′-末端结合口袋,还发现了新的G偏好口袋,形成了决定切割定位的双口袋机制。这一发现为理解DICER处理多样化RNA底物提供了新框架,其意义超越基础生物学,有望推动RNA疗法改进、基因沉默技术优化及遗传疾病机制研究。”
出版详情:作者:Hong Kong University of Science and Technology,标题:《How DICER cuts microRNAs with single-nucleotide precision》,发表于:《Nature》(2026)。
