胰腺癌是一种难治的恶性肿瘤,常因诊断较晚导致手术不可行,生存率较低。最常见的胰腺导管腺癌(PDAC)被促结缔组织增生基质所包围,这是一种由结缔组织和癌症相关成纤维细胞(CAFs)组成的致密屏障,会抑制免疫反应,并限制嵌合抗原受体(CAR)T细胞疗法的应用,而CAR-T疗法在血液癌症如淋巴瘤中已获成功。
宾夕法尼亚大学兽医学院的研究团队,由癌症中心主任Ellen Puré领导,使用脂质纳米颗粒(LNPs)作为递送系统,在临床前模型中生成靶向CAFs的CAR T细胞,以“融化”这一屏障。研究结果发表在《癌症免疫学研究》上,为CAR-T疗法治疗实体瘤提供了更安全、易获取且成本效益高的新途径。Puré表示:“CAR-T的扩展非常巨大,但它们实际上只在液体肿瘤中取得成功。”传统CAR-T疗法过程复杂,需提取和改造患者T细胞,而基于LNP的方法可能更简便。
团队利用LNPs将CAR指令直接递送至患者T细胞,靶向成纤维细胞活化蛋白(FAP),这在CAFs亚群上高水平表达,对PDAC进展至关重要。高级研究员Khuloud Bajbouj解释:“这就像为T细胞配备了激光聚焦的方法。”Puré补充,他们选择FAP因之前研究显示靶向这些细胞可延迟肿瘤生长。
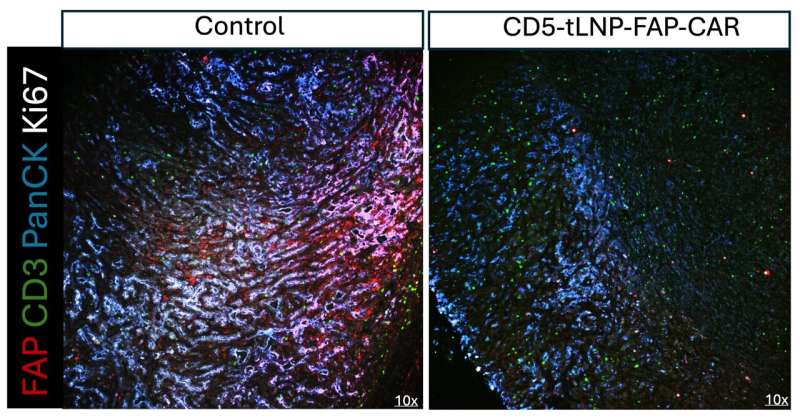
在PDAC临床前模型中,单剂量靶向LNPs(tLNPs)在抑制肿瘤生长方面与传统方法相当或更优。Puré指出:“通常只有不到10%进入肿瘤的T细胞被武装起来,但使用tLNPs时,40%到60%的T细胞表达了CAR。”这些武装T细胞存在时间较短,但效果显著,甚至让研究人员惊讶于基质的“融化”。
Bajbouj说,这为联合疗法铺平道路,可与化疗或免疫疗法结合以提高实体瘤疗效。Puré表示:“一旦大门打开,许多疗法都可以进入并表现良好。”数据还显示,该方法可能对转移性癌症有效,Puré补充,转移是多数癌症患者死亡原因。
研究认为,靶向FAP阳性细胞有潜力超越胰腺癌,治疗纤维化、自身免疫病等疾病。Puré总结:“从风险-收益的角度来看,tLNP mRNA方法可能更容易被接受。”脂质纳米颗粒的应用有望推动CAR-T疗法在实体瘤中的发展。
出版详情:作者:University of Pennsylvania;标题:《Targeting tumor supporting cells: Lipid nanoparticles advance CAR T success in pancreatic cancer》;发表于:《Cancer Immunology Research》(2026)。
