中国台湾科学家开发了一种精密纳米平台,用于治疗胶质母细胞瘤(GBM),这是一种侵袭性较强的脑癌。治疗胶质母细胞瘤通常面临肿瘤弥漫性浸润、血脑屏障(BBB)阻隔以及复杂肿瘤微环境的挑战。癌症相关成纤维细胞(CAFs)是这种微环境的关键组成部分,它们支持肿瘤生长并抑制免疫系统。
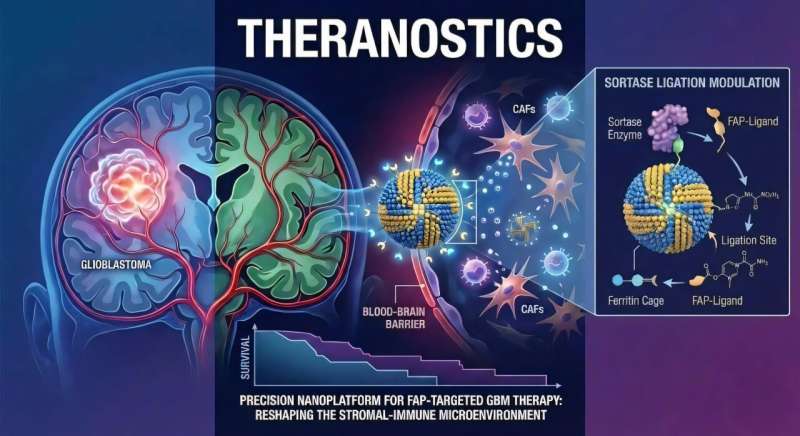
在《Theranostics》期刊发表的一项新研究中,来自国立台湾大学和林口长庚纪念医院的团队揭示了一种基于铁蛋白的模块化药物载体(FDC)方法。该载体利用成纤维细胞活化蛋白(FAP)作为靶点,FAP在CAFs和胶质母细胞瘤细胞中均有表达,为药物递送提供了全面靶向机会。
研究人员通过位点特异性Sortase A介导的连接技术,将优化的FAP靶向配体附着在铁蛋白壳表面,同时保持其天然结构和载药能力。在工程化纳米笼内,团队封装了强效细胞毒素单甲基奥瑞他汀E(MMAE),形成双靶向纳米载体。这种载体利用铁蛋白与转铁蛋白受体1(TfR1)结合的自然能力,同时靶向FAP以消除肿瘤细胞及其基质支持。
在原位胶质母细胞瘤小鼠模型中测试时,该靶向方法显示出较高精确性。载体采用pH响应机制,在血流中保持稳定,进入肿瘤酸性微环境后迅速释放MMAE有效载荷。与游离MMAE相比,这种方法增强了细胞摄取、减少了肿瘤负荷并延长了生存期,同时最小化了对健康脑组织的损伤和全身毒性。
研究第一作者、国立台湾大学研究员曾毅祥表示:“我们的方法结合了制导导弹和特洛伊木马策略。通过使用天然蛋白质进入大脑,并添加肿瘤发现功能,我们可以将强效药物精确投放到癌症区域,确保健康组织安全。”
利用空间转录组学分析和免疫组织化学,研究人员发现该靶向疗法能重塑肿瘤微环境。通过同时攻击CAFs和肿瘤,治疗打破了肿瘤防御基质,弥合了肿瘤与免疫系统之间的间隙。这种调节成功招募了细胞毒性免疫细胞深入肿瘤,激活了多个免疫通路,将免疫抑制环境转变为反应性环境。
研究团队计划基于对胶质母细胞瘤基质-免疫动力学的新见解,持续优化这一模块化平台。最终目标是将CAF调节技术与现有免疫疗法结合,为患者提供持久治疗方案。
共同通讯作者、国立台湾大学生化科学与技术系副教授黄丰廷博士指出:“这个平台为脑癌治疗开辟了新方向。通过设计双靶向载体突破血脑屏障并招募免疫细胞,我们正在将‘免疫冷’肿瘤转变为‘热’肿瘤,为患者带来变革性希望。”
出版详情:作者:National Taiwan University;标题:《Scientists engineer a 'Trojan Horse' to conquer aggressive brain cancer》;发表于:《Theranostics》(2026)。
