脊髓延髓肌萎缩症(SBMA)是一种罕见的遗传性神经退行性疾病,主要影响男性,导致进行性肌肉无力和萎缩。患者通常在30多岁时出现早期症状如手部震颤,但诊断常在40岁左右肌肉无力明显时。该病由高水平睾酮引发,因此仅男性受累。
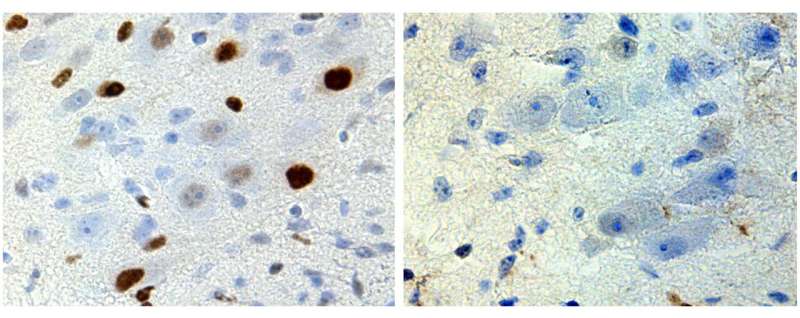
名古屋大学的研究团队在《自然通讯》发表研究,揭示出生后不久睾酮的自然激增会触发SBMA的早期病理过程。在携带SBMA突变的新生小鼠中,睾酮激增导致突变蛋白过度激活控制肌肉的神经细胞(运动神经元),最终引发成年期神经细胞崩溃。出生时治疗可显著减少这种崩溃,为早期干预提供新思路。
所有新生男性都会经历短暂睾酮激增,称为“微型青春期”,在小鼠中持续约10天,人类中约六个月。由于SBMA的缺陷蛋白——突变雄激素受体蛋白——需要睾酮进入运动神经元细胞核造成损伤,这次激增被视为疾病触发的最早时刻。研究主要作者平木知树助理教授表示:“我们证实,在雄性SBMA小鼠出生第一天,突变蛋白就在运动神经元细胞核积累,而雌性小鼠无此效应,证实睾酮是关键触发因素。”在SBMA小鼠出生第一周,负责激活神经细胞的基因异常活跃,导致运动神经元过度活跃,这一现象在人类患者细胞培养中也观察到,提示人类疾病过程可能类似。
为测试早期治疗,研究人员对新生SBMA小鼠使用两种基因沉默药物:一种靶向突变蛋白,另一种靶向REST4蛋白,后者驱动异常神经细胞过度活跃。靶向突变蛋白的药物暂时降低蛋白水平,靶向REST4的药物纠正异常基因活动。两种治疗均改善小鼠13周龄时的存活率、运动表现,并减少运动神经元退化。平木博士指出:“出生时给予的药物在数月后仍保护运动神经元,即使药效已消失,表明早期干预可产生持久效果。”REST4蛋白成为未来治疗潜在新靶点,名古屋大学此前开发的醋酸亮丙瑞林是日本唯一批准用于SBMA的药物,这些发现延续了该校在该疾病的研究传承。
研究团队下一步将确认人类SBMA患者中是否发生类似异常神经细胞过度活跃,并评估基因沉默药物的安全性和重复治疗效应。平木博士强调:“直接研究活体患者新生儿神经系统活动不可行,但目标是将发现转化为患者护理。”这项研究为脊髓延髓肌萎缩症的早期诊断和治疗开辟新途径,强调生命早期关键窗口期的重要性。
出版详情:作者:Nagoya University;标题:《Treating disease at birth: How a brief spike in testosterone sets the trajectory for disease that appears decades later》;发表于:《Nature Communications》(2026)。
