德国拜罗伊特大学的科研团队在《自然通讯》杂志上发布了一项重要研究成果,首次揭示了潜在抗癌药物fostriecin生物合成过程中的关键机制。由Frank Hahn教授领导的团队在实验室中成功制备了所有相关酶,并在受控环境下进行了独立分析,为更高效生产这种化合物奠定了基础,有望推动癌症治疗新方法的开发。
Fostriecin是一种由细菌产生的天然产物,能够通过干扰信号通路促使癌细胞死亡。然而,先前临床试验因无法获取足够数量和纯度的该物质而中断,其不稳定性与结构特性也增加了药物研发难度。此次研究聚焦于药效团——即分子中决定药理活性的核心部分,旨在克服这些障碍。
Hahn教授表示:“我们首次在实验室中合成了多种对构建fostriecin药效团至关重要的酶,并在细胞外条件下进行了单独研究。”研究人员还证实,当这些酶在单一容器中结合时,它们能协同作用形成药效团。Hahn补充说:“这对于现代合成技术发展具有积极意义,因为经济和环境因素促使人们寻求以更少资源生产复杂分子的方法,酶促合成在这方面潜力显著。”
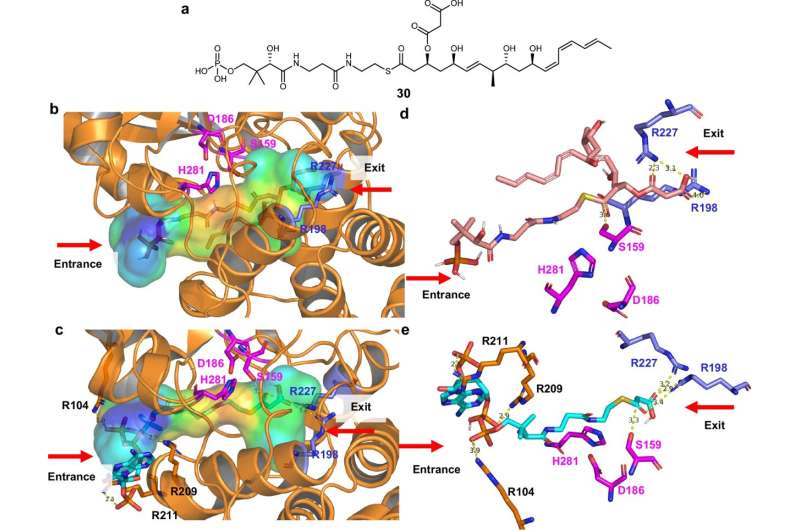
研究中的一个新发现是识别了之前未知的酶活性:一种硫酯酶在药效团形成中承担转移丙二酸和构建环状结构的双重任务,而一种新型脱丙二酰酶则移除丙二酸,生成与癌细胞靶蛋白相互作用的部分。药效团的成功构建依赖于硫酯酶、脱丙二酰酶和激酶之间的精确配合,激酶负责引入特征性磷酸酯。
Hahn解释说:“这种协调优化了生物活性终产物的生成。若无这三种酶的精准协作,细菌中的fostriecin生物合成途径就像漏水的软管:尽管投入大量资源,却常因产生非活性和不稳定的中间体而无法得到所需分子。”未来,团队计划将这一见解应用于结构类似天然产物的生物合成,并利用已识别的酶进行靶向化学酶促合成,结合合成化学与生物技术优势,进一步提升药物开发效率。
出版详情:作者:Theresa Hübner, Bayreuth University;标题:《Why a potential anti-cancer agent stalled in trials: New enzyme insights may boost yield and purity》;发表于:《Nature Communications》(2026)。
