嵌合抗原受体T细胞疗法(CAR T)在治疗血液癌症方面已取得进展,但对抗实体瘤面临挑战,包括缺乏一致性靶点和免疫抑制微环境。美国纪念斯隆凯特琳癌症中心的研究人员开发了一种新型CAR T细胞,通过靶向uPAR蛋白同时攻击癌细胞和肿瘤支持细胞,临床前结果发表在《细胞》杂志上。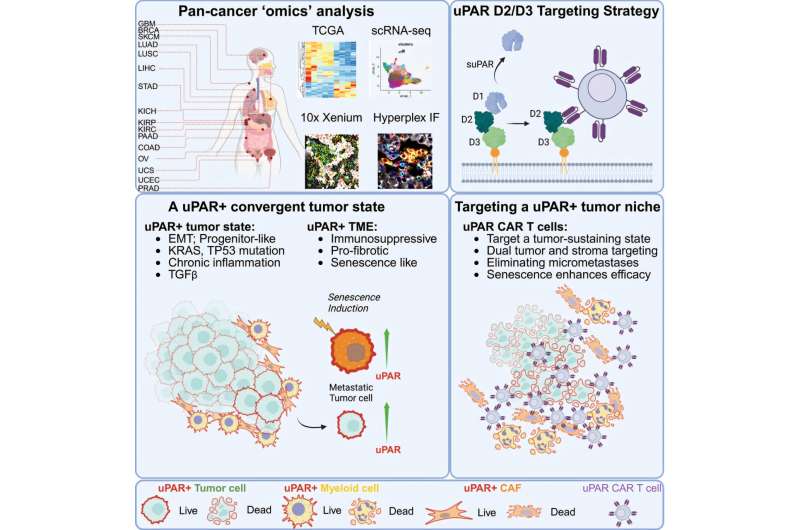
该研究由Zeda Zhang博士领导,资深作者包括Scott Lowe博士、Michel Sadelain博士和Aveline Filliol博士。Lowe博士表示:“这种方法在实验室中缩小了肺癌、胰腺癌和卵巢癌等实体瘤,甚至清除了转移灶。”他补充道:“工程细胞选择性消除肿瘤细胞和uPAR阳性支持细胞,破坏肿瘤保护环境。”
在卵巢癌小鼠模型中,靶向uPAR的CAR T细胞清除转移灶,实现持久缓解,并抵抗新肿瘤发展。手术后单次辅助剂量也能消除残留病灶,优于单独手术。
uPAR是一种细胞表面蛋白,在健康组织中少见,但在癌症中高表达于肿瘤细胞和微环境细胞。研究人员通过关注uPAR,靶向特定状态细胞,而非特定类型。张博士指出:“uPAR标记恶性肿瘤和更广泛的生态系统,这是其独特之处。”
研究发现,在14种人类癌症中,12种uPAR升高,尤其在卵巢癌、胰腺癌、结肠癌、肺癌和脑癌中。Filliol博士说:“高uPAR表达与p53突变、KRAS激活及侵袭性癌症标志相关。”临床前实验中,结合化疗如顺铂可增强效果,当细胞表面至少有1,500个uPAR分子时疗效最佳。
Sadelain博士强调:“uPAR导向的CAR T细胞从多角度攻击肿瘤,靶向肿瘤细胞和支持细胞。”Lowe博士认为,这反映了肿瘤进展涉及生态系统互动。此外,靶向uPAR在纤维化等疾病中也有前景,并可通过血液检测和PET扫描监测。
出版详情:作者:Memorial Sloan Kettering Cancer Center;标题:《uPAR-targeted CAR T cells shrank solid tumors and cleared metastases in mice》;发表于:《Cell》(2026);期刊信息:《Cell》。
