心脏作为人体重要器官,每天持续跳动约10万次,其能量主要来源于线粒体。线粒体产生身体所需95%的三磷酸腺苷(ATP),是细胞的关键能量来源。若线粒体功能受损,心肌细胞将无法有效泵送血液和营养物质。
心脏在所有器官中拥有最高的线粒体密度,约占细胞体积的三分之一。在发育过程中,线粒体需要迁移到肌节位置以支持心肌收缩。德国汉诺威医学院(MHH)的研究团队由Christian Riehle博士和Johann Bauersachs教授领导,发现RHOT蛋白在控制线粒体运动方面起关键作用。这一发现可能为心力衰竭等心脏疾病提供新的治疗方向。相关研究成果已发表于《Circulation Research》期刊。
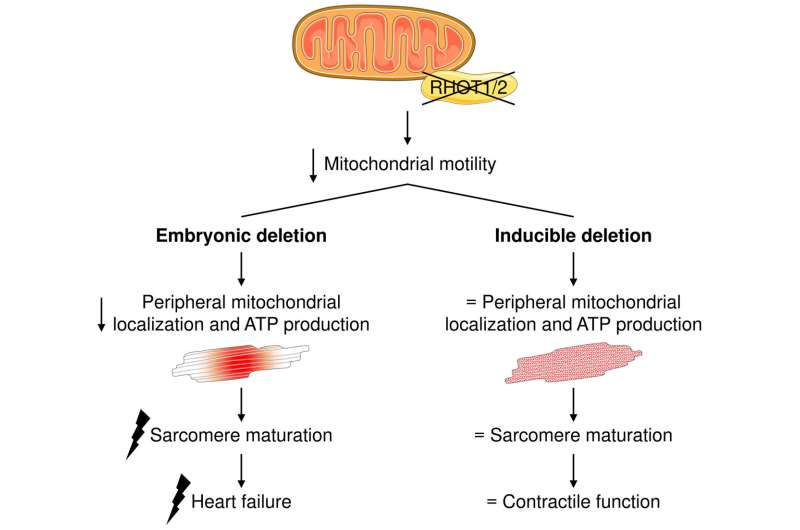
研究团队通过基因分析识别出心脏中高表达的RHOT1和RHOT2蛋白。Christian Riehle博士表示:“心脏中产生大量的RHOT1和RHOT2,它们的高丰度表明其负责关键机制。”在胚胎发育期间敲除这些蛋白后,Natali Froese博士指出:“线粒体没有迁移到肌节,而是聚集在细胞核周围。”这导致肌节能量供应不足,引发心脏发育障碍和心力衰竭。
在成年小鼠中,RHOT蛋白的缺失对线粒体位置影响较小,因为线粒体已定位。然而,在心脏承受额外压力时,如心脏病发作后,RHOT蛋白的作用变得重要。Christian Riehle博士解释:“在这种情况下,RHOT蛋白代表了一个有吸引力的治疗靶点。”通过增加RHOT蛋白活性,可能提升心肌细胞能量供应,基因治疗是潜在方法之一。
RHOT蛋白在围产期心肌病(PPCM)治疗中也有应用前景。怀孕期间心肌扩大可能增加心脏负担,RHOT蛋白调控有助于减轻压力。Johann Bauersachs教授强调:“RHOT蛋白也可以在这里提供一个治疗方法,以减轻孕妇心肌细胞的压力并保护心脏。”这项研究为心脏疾病治疗开辟了新途径,聚焦于能量供应机制的优化。
出版详情:作者:Inka Burow, Hannover Medical School;标题:《How RHOT proteins regulate energy supply in heart muscle cells》;发表于:《Circulation Research》(2026);期刊信息: Circulation Research。
