美国FDA批准Lantheus公司Pylarify TruVu新制剂,提升前列腺癌PSMA PET显像可及性
2026-03-08 14:09
收藏
美国食品药品监督管理局(FDA)近日批准了Pylarify TruVu™,这是前列腺特异性膜抗原(PSMA)正电子发射断层扫描(PET)显像剂Pylarify(piflufolastat F 18)的一种新配方。这一决定旨在优化前列腺癌诊断工具的稳定性和生产效率。
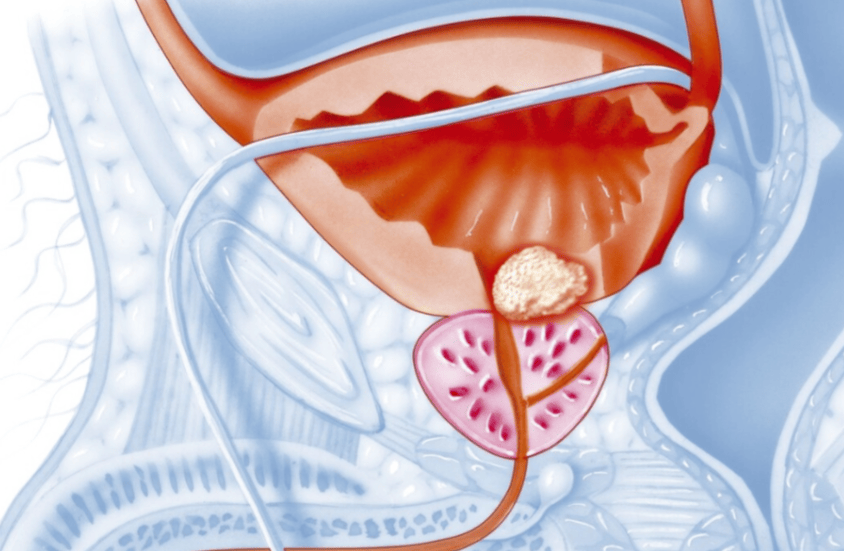
根据开发商Lantheus公司的说明,Pylarify TruVu适用于PSMA PET显像,主要针对因前列腺特异性抗原(PSA)水平升高而疑似前列腺癌复发,或怀疑存在转移且适合初始根治性治疗的男性患者。新制剂增强了piflufolastat F 18在更高放射性浓度下的稳定性,从而支持更高的制造效率和更大的生产规模,这可能有助于改善患者对PSMA PET显像剂的获取。
Lantheus公司执行主席兼首席执行官玛丽·安妮·海诺表示:“FDA对Pylarify TruVu的批准展示了Lantheus公司持续致力于推进创新,直接扩大患者获取高质量诊断工具的机会。”
前列腺癌基金会总裁兼首席执行官吉娜·B·卡里瑟斯补充说:“随着前列腺癌发病率预计在未来几年上升,看到像Lantheus这样的公司以患者为先,推出有助于确保及时、精确显像的创新,同时跟上不断增长的需求,令人鼓舞。获取准确的诊断,尤其是在怀疑转移或复发疾病时,能深刻影响前列腺癌患者的生活质量和长期结果。”这一进展有望为前列腺癌患者提供更可靠的PSMA PET显像选项。
相关推荐
罗氏六天开发检测本迪布焦病毒的PCR方法
2026-06-08
巴西Ávita Care争取6月内获批司美格鲁肽减肥笔
2026-06-08
丹麦Zealand公司2期试验减重10.7%
2026-06-08
英国汉莎Idefirix肾移植达90%一年无移植物衰竭生存
2026-06-08

美卫生部长推动获取医疗记录研究疫苗自闭症
2026-06-08
法国Abivax UC药III期阳性现安全信号
2026-06-08

德国研究:耻骨联合旁骨髓水肿患病率11.1%,裂隙征6.0%
2026-06-08

迪拜Lueur诊所报告透明质酸填充剂致血管阻塞病例
2026-06-08

美国阿帕他胺围术期治疗降低高危前列腺癌远处转移或死亡风险20%
2026-06-08

菲律宾Kutis by Kei诊所扩张 新设7间治疗室及德国激光平台
2026-06-08