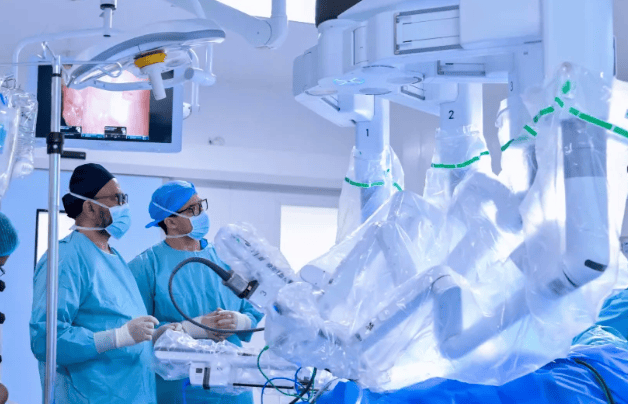
在比利时比尔瑟,2026年3月10日强生公司宣布,已向欧洲药品管理局(EMA)提交了一项II型变更申请,旨在将TECVAYLI®(teclistamab)作为单药疗法,用于治疗既往至少接受过一线治疗的成人复发/难治性多发性骨髓瘤(RRMM)患者。
多发性骨髓瘤的一线治疗虽已取得进展,但多数患者仍会复发。一旦对关键疗法如抗CD38单克隆抗体和来那度胺耐药,预后较差。这一患者群体治疗选择有限,亟需更多有效免疫疗法。
强生公司欧洲、中东和非洲(EMEA)治疗领域负责人、血液学专家Ester in 't Groen表示:“大量多发性骨髓瘤患者持续复发并对现有疗法产生耐药,这代表了该疾病中最大且最具挑战性的未满足需求之一。将teclistamab单药疗法尽早用于二线治疗,有可能显著改善长期预后并改变疾病进程,这可能为患者及其家庭带来新希望。”
Teclistamab单药疗法的安全性特征在临床上可控,未发现新的安全信号。感染可通过稳健的感染管理方案控制。独立数据监测委员会基于首次预设中期分析的数据强度,建议揭盲该研究。此次提交是计划中多项全球监管申报的首个,完整结果将在未来的重要医学会议上公布。
强生公司多发性骨髓瘤疾病领域负责人、医学博士Jordan Schecter表示:“在强生公司,我们秉持明确的目标,致力于提供创新,重新定义多发性骨髓瘤诊断对患者在每个疾病阶段的意义。随着teclistamab今日达到这一监管里程碑,我们正在推进一种广泛可用的免疫疗法方法,其有潜力随时间推移支持深入且持久的反应。”
Teclistamab于2022年8月获得欧盟委员会(EC)批准,用于治疗既往至少接受过三种疗法的RRMM患者。2023年8月,EC批准了teclistamab的II型变更申请,为达到完全缓解至少六个月的患者提供了减少给药频率选项。Teclistamab是一种即用型双特异性抗体,通过两个细胞靶点(BCMA和CD3)重定向T细胞,激活人体免疫系统对抗癌症。