美国PathAI公司AI皮肤病理学工具获FDA突破性设备认定
2026-03-06 11:09
收藏
美国食品和药物管理局(FDA)近日授予PathAI公司的人工智能驱动皮肤病理学工作流程解决方案PathAssist Derm突破性设备认定。这一工具专注于评估皮肤病理学病变的数字病理学全切片图像,为病理学家提供审查辅助。
PathAssist Derm旨在利用人工智能技术应对皮肤病理学中的诊断挑战。在美国皮肤癌发病率上升的背景下,病理学家面临显著的观察者间变异问题,尤其是在黑素细胞病变的诊断中。一项研究显示,在部分复杂病变类别中,诊断准确性和一致性低于50%。
PathAI首席执行官Andy Beck博士表示:“这一认定是对我们AI能力和承诺的有力认可,我们致力于将经过严格验证、临床相关的工具引入数字病理学领域。”他还指出:“通过与FDA在突破性设备计划中的紧密合作,我们的目标是加速开发和审查过程,确保这项变革性技术尽快到达病理学家和患者手中。”
PathAI近期已取得多项监管进展,包括获得AISight Dx的510(k)许可,这是首个带有授权预定变更控制计划的数字病理学图像管理系统。此外,该公司还获得了欧洲药品管理局(EMA)和FDA对AIM-MASH AI Assist的资格认定,作为首个AI驱动的病理学药物开发工具。
PathAssist Derm通过AI支持病例评估和工作流程优先级排序,帮助病理学家管理日益增加的工作量,同时提升诊断效率。该工具于2025年2月推出,专为定向、检测和测量皮肤病变而设计,并可在AISight图像管理系统上使用。
PathAI公司表示将继续与全球监管机构合作,推进AI驱动的病理学解决方案,以增强诊断信心并支持患者护理。这一突破性设备认定有望加速PathAssist Derm的临床应用进程。
相关推荐

澳大利亚布莱顿健康校园新增一间医学影像科
2026-06-04
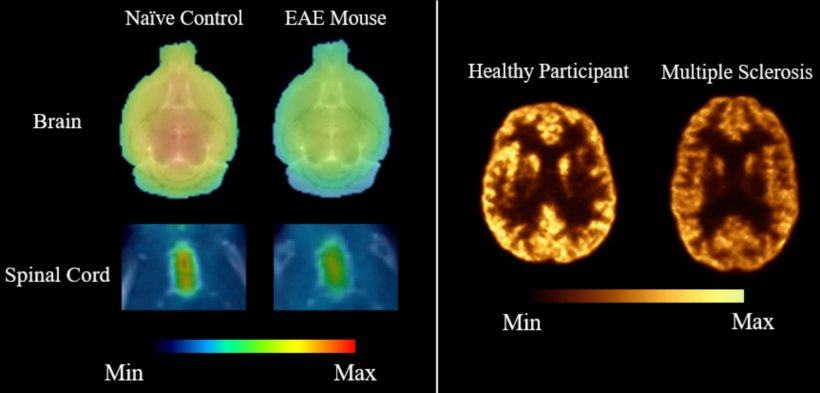
加拿大研究:PET成像揭示多发性硬化突触密度降低16.4%
2026-06-04
英国阿尔德利公园7.1万平方英尺建筑将改建为私立医院
2026-06-04

英国Flok Health获1250万美元融资拓展AI理疗平台
2026-06-04

英国QCS收购CareBrain加速护理行业转型
2026-06-04

美国加州大学与英国牛津大学开发可穿戴超声贴片实现持续胎儿监测
2026-06-04

新加坡Angel Eye引入AI视网膜筛查助术前评估
2026-06-04

突尼斯实现前列腺癌关键放射性药物本土生产
2026-06-04
法国团队开发出Otosurg 3D打印耳部手术模拟器
2026-06-04

美国量化路径新增斯蒂芬斯博士扩充食品安全团队
2026-06-04