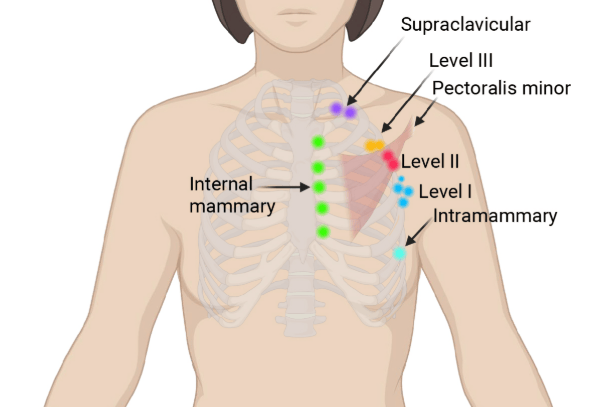
英国医学研究委员会(MRC)医学科学实验室的Louise Fets博士团队在《自然通讯》发表研究,利用质谱成像和空间转录组学技术分析患者卵巢肿瘤样本,揭示了PARP抑制剂在肿瘤内分布不均的机制。研究发现,这些靶向药物会在细胞内的溶酶体中积累,形成“隐藏的药物仓库”,影响治疗效果。
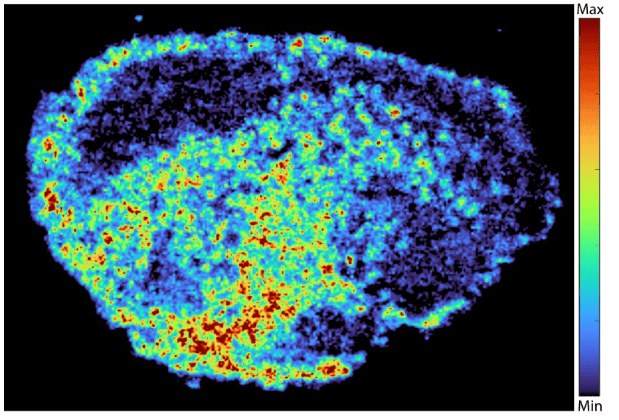
研究人员使用从患者体内取出并在实验室中保持活性的卵巢肿瘤薄切片,通过处理PARP抑制剂,直接观察药物在真实人类肿瘤组织中的扩散情况。质谱成像技术创建了高分辨率图谱,精确显示药物分子的积累位置,结合空间转录组学分析,比较了同一组织样本中药物水平高和低区域的基因活性差异。
结果显示,即使使用相同剂量,同一肿瘤的不同区域以及不同患者之间的药物水平存在显著差异。团队发现,这种不均匀分布是由溶酶体驱动的,部分PARP抑制剂如rucaparib和niraparib被拉入溶酶体存储,形成内部储库,像缓释仓库一样捕获和释放药物,导致某些细胞暴露增加,而其他细胞相对未暴露。
“这项研究的一个新颖方面是使用质谱成像直接测量和可视化患者肿瘤组织中的药物摄取。通过药物分子的空间映射,我们能够精确定位药物高和低的区域,并使用空间转录组学比较来自同一组织切片的基因表达,”资深作者、帝国理工学院代谢、消化与生殖系副教授Zoe Hall博士说。
第一作者、LMS博士后研究员Carmen Ramirez Moncayo博士补充道:“我们惊讶地看到单细胞水平上药物积累的巨大变异性。这种变异性是由药物在溶酶体中的积累驱动的,溶酶体充当储库,通过存储和在需要时释放药物,增加癌细胞对药物的暴露。”
PARP抑制剂已广泛用于卵巢癌、乳腺癌和前列腺癌治疗,并正在许多其他癌症的临床试验中。了解药物在细胞中的存储和分布机制,可能为个性化治疗策略提供新思路,有助于提高成功率并减少耐药性或复发。
资深作者Louise Fets博士指出:“通过了解药物如何被细胞摄取,我们可以理解这是否影响为什么癌症药物对某些人有效而对其他人无效。最终,我们希望能够研究患者肿瘤的分子特征,以帮助以更个性化的方式定制治疗方法。”
这项研究使用了体外维持的患者肿瘤组织,未来将扩展到动物模型和更大规模的患者研究,以探索在真实临床环境中药物输送、肿瘤结构和溶酶体存储的相互作用。研究获得医学研究委员会、英国癌症研究等机构的资金支持。