BD获FDA批准EnCor EnCompass乳腺活检系统
2026-01-20 11:55
收藏
医疗技术企业BD宣布其EnCor EnCompass乳腺活检及组织切除系统获美国食品药品监督管理局(FDA)510(k)批准,预计于2026年初正式上市。这一多模态系统整合了可调节样品缺口、360°采样能力及多规格探针(10G/7G/12G)等创新功能,支持跨超声、X光等乳腺成像平台的无缝切换,旨在简化活检流程并提升临床诊断效率。
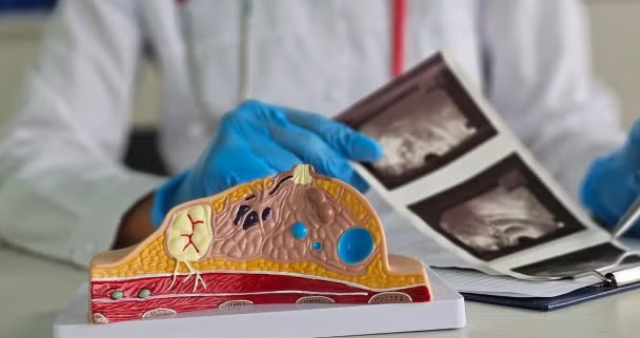
EnCor EnCompass系统的核心优势在于其灵活性设计。设备配备高低真空强度调节功能,搭配回声切割导管实现精准可视化操作,同时提供带照明的样品容器以优化组织取样质量。BD周围周边干预全球总裁Rima Alameddine表示:“该系统标志着乳腺健康领域的重要进展,通过集成多模态技术,我们为临床医生提供了更高效的诊断工具,助力乳腺癌的早期发现与干预。”
技术团队强调,系统开发过程中深度融合了临床反馈。介入性-外围干预肿瘤平台副总裁Stacie Watson指出:“我们持续关注医生与患者的动态需求,EnCor EnCompass的模块化设计兼顾了操作控制性与用户体验,例如其兼容性可减少设备切换时间,而多样化的探针选项则能适配不同病变类型。”FDA的批准进一步扩展了BD在乳腺健康领域的技术布局,强化了其从筛查到诊断的全周期解决方案能力。
FDA的批准与BD近期在医疗制造领域的战略投入形成协同。2025年8月,该公司宣布投资超3500万美元扩建美国内布拉斯加州哥伦布工厂的预加式冲洗注射器产能,凸显其通过本地化生产强化供应链韧性的决心。
相关推荐
中国LongBio Pharma港股上市市值107亿港元
2026-06-06

中国海尔在上海老博会推出三大AI陪伴机器人
2026-06-06

丹麦Veeva峰会展示Falcon平台及Vault AI计划
2026-06-06
加拿大Rakovina一季度研发支出占比升至70%
2026-06-06

美国Commure获7000万美元融资估值70亿
2026-06-06

美国WellSpan Health与飞利浦达成七年战略合作
2026-06-06

英国圣玛丽医院公布20亿英镑重建规划图
2026-06-06

美国AltesaASM会议公布vapendavir 2a期研究
2026-06-06

法国赛诺菲与Owkin扩大AI合作构建药物开发智能体
2026-06-06

美国堪萨斯州拨款近8000万美元资助39家机构加强农村医疗
2026-06-06