Opna Bio扎瓦布雷西布获FDA孤儿药资格,推进骨髓纤维化治疗研究
2026-01-22 15:42
收藏
Opna Bio近日宣布,其试验性疗法OPN-2853(国际非专有名称:扎瓦布雷西布)已获得美国食品药品监督管理局(FDA)授予的孤儿药资格,用于治疗罕见血癌骨髓纤维化。该药物是一种针对溴结构域和超末端(BET)蛋白的小分子抑制剂,目前正通过联合用药策略探索其在骨髓纤维化治疗中的潜力。
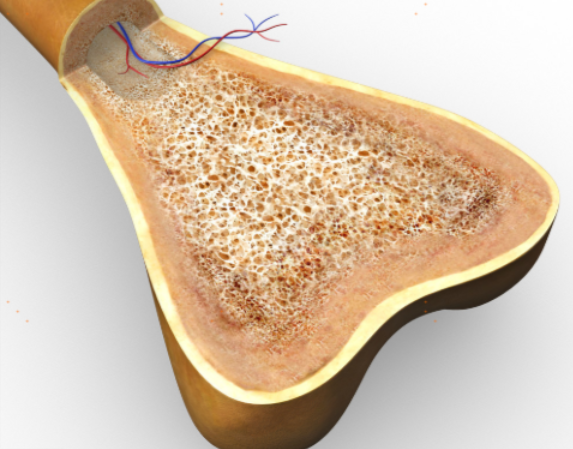
骨髓纤维化是一种影响骨髓正常造血功能的罕见疾病,美国约有2.5万名患者,常见症状包括疲劳、贫血及脾脏肿大。扎瓦布雷西布目前处于一期临床试验阶段,作为鲁索替尼的附加治疗,针对已对鲁索替尼单药治疗产生耐药性的患者。2025年底公布的研究数据显示,接受联合治疗的可评估患者中,多数脾脏体积显著缩小,初步验证了其疗效潜力。
孤儿药资格的授予为扎瓦布雷西布的临床开发提供了多项激励,包括税收抵免、监管费用减免及获批后可能的市场独占权。Opna Bio表示,这一认定将加速药物研发进程,并计划未来开展更多临床研究,以全面评估扎瓦布雷西布作为骨髓纤维化新治疗选择的长期安全性与有效性。
作为BET蛋白抑制剂领域的创新药物,扎瓦布雷西布的研发得益于英国学术与研究机构的合作支持。其作用机制通过靶向癌细胞增殖相关蛋白,为传统疗法耐药的骨髓纤维化患者提供了新的治疗路径。
相关推荐
罗氏六天开发检测本迪布焦病毒的PCR方法
2026-06-08
巴西Ávita Care争取6月内获批司美格鲁肽减肥笔
2026-06-08
丹麦Zealand公司2期试验减重10.7%
2026-06-08
英国汉莎Idefirix肾移植达90%一年无移植物衰竭生存
2026-06-08

美卫生部长推动获取医疗记录研究疫苗自闭症
2026-06-08
法国Abivax UC药III期阳性现安全信号
2026-06-08

德国研究:耻骨联合旁骨髓水肿患病率11.1%,裂隙征6.0%
2026-06-08

迪拜Lueur诊所报告透明质酸填充剂致血管阻塞病例
2026-06-08

美国阿帕他胺围术期治疗降低高危前列腺癌远处转移或死亡风险20%
2026-06-08

菲律宾Kutis by Kei诊所扩张 新设7间治疗室及德国激光平台
2026-06-08