细胞凋亡过程中释放的膜囊泡是重要生物学事件,其中凋亡囊泡(ApoVs)作为一种新发现的小型囊泡,不仅继承母细胞特性,还在疾病诊疗中具有应用潜力。实时监测ApoV形成过程,包括数量、形态与释放动态,有助于解析凋亡调控机制并优化制备策略,但传统荧光染料与诱导方法存在局限,难以全面动态追踪。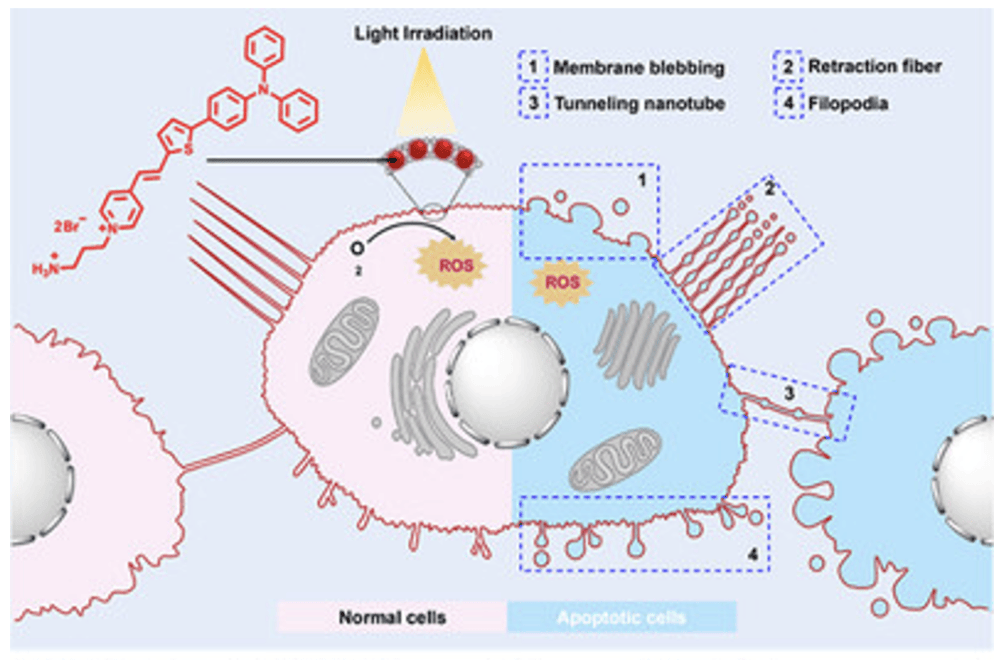
具有聚集诱导发光(AIE)特性的有机光敏剂为解决此问题提供了新途径。这类分子可通过结构修饰靶向质膜(PM),在光照下高效产生活性氧(ROS),从而加速凋亡过程,克服传统方法的延迟与非特异性问题。同时,AIE光敏剂凭借高荧光量子产率、低背景干扰和优异光稳定性,成为质膜长期动态成像的理想选择,为同时诱导凋亡并监测ApoV形成全过程提供了工具。
山东大学余小强、刘志强与山东省耳鼻喉医院牛杰等研究人员合作,开发了一种名为ADTP的多功能AIEgen,专门用于监测ApoV形成过程。ADTP以三苯胺荧光团作为电子供体,噻吩单元扩展π共轭体系,亲水性双盐基团兼具PM靶向与电子受体功能,在光照下表现出色ROS生成效率,能同时产生I型和II型ROS。
在细胞实验中,ADTP特异性靶向质膜,并在激光照射下高效诱导凋亡,使荧光显微镜能连续记录整个ApoV形成过程。研究发现,ApoVs来源于多种膜突起,如丝状伪足、隧道纳米管和回缩纤维,这些突起可能通过不同机制促进ApoV形成。
ADTP的近红外发射与配备775 nm耗尽激光的受激发射损耗(STED)显微镜兼容,可实现高分辨率成像,清晰可视化ApoV形成过程中的细微膜重塑动态。通过调节细胞条件诱导肌动蛋白或微管蛋白主导的膜突起,STED成像显示,富含肌动蛋白的突起倾向于产生小而分散的ApoVs,而富含微管蛋白的突起则生成更大、可融合的ApoVs。
研究人员表示,这些高分辨率图像证明了ADTP作为光学工具在监测来自不同膜突起的ApoVs方面的有效应用。该工作为监测完整ApoV形成过程提供了强大工具,并为阐明ApoV形成机制提供了关键证据,有望推动相关生物医学研究进展。