在《自然通讯》发表的一项研究中,威斯康星大学麦迪逊分校的研究人员介绍了一种深度学习方法,能够自动识别蛋白质构象变化中的过渡态,这是支撑许多生物功能的关键过程。
这种新工具有望加速生物分子动力学的研究,并可在药物设计、生物分子工程和材料科学领域得到广泛的应用。
这项研究是威斯康星大学麦迪逊分校化学系黄旭辉教授团队与计算机科学系 Sharon Li 教授团队合作的成果。
过渡态识别长期以来被认为是化学领域的“圣杯”。与化学反应不同,生物分子构象变化(例如蛋白质折叠或与其他分子结合)涉及多个亚稳态中间态,从而在复杂的结构中,在自由能垒处产生众多过渡态。
尽管经过数十年的研究,现有方法仅能定位亚稳态对之间的过渡态。同时自动识别生物分子过程中的所有过渡态仍然是一项重大挑战。
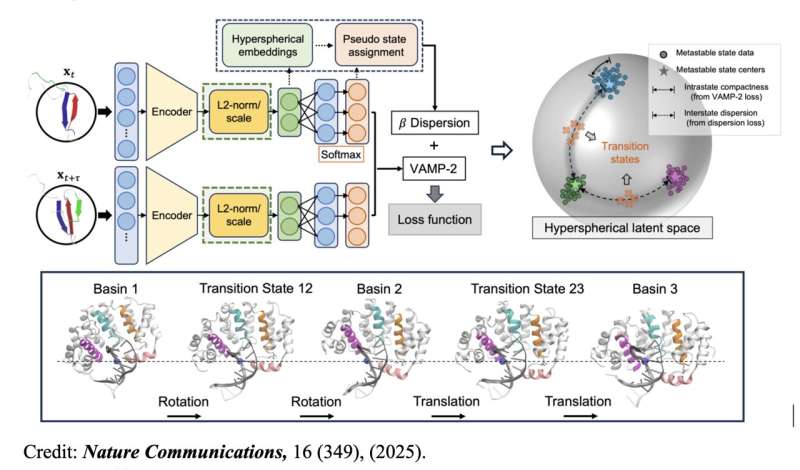
这项新技术名为 TS-DAR(通过色散和变分原理正则化神经网络进行过渡态识别),它利用受分布外(OOD)检测启发的深度学习框架克服了这些挑战。分布外(OOD)检测是人工智能(AI)中用于识别偏离典型模式的数据的概念。
TS-DAR 的关键突破在于它能够将过渡态视为 OOD 数据——位于亚稳态构象之间自由能垒处的稀有结构。该方法的工作原理是将分子动力学(MD) 数据嵌入到超球面潜空间中,从而有效地检测和分离这些稀疏分布的过渡态。
该方法为研究蛋白质动力学和识别生物分子过程中涉及的所有过渡态提供了全面的端到端流程。
黄旭辉教授表示:“识别过渡态是研究蛋白质动力学中最具挑战性和最重要的任务之一。TS-DAR 是第一种能够从 MD 数据中自动一次性捕获所有过渡态的方法,从而能够更深入地理解潜在的分子过程。”
研究团队在一系列系统上测试了 TS-DAR,包括 DNA 马达蛋白 (AlkD) 沿 DNA 的易位。在每种情况下,TS-DAR 在准确性和效率方面均优于传统方法。
值得注意的是,在 AlkD 系统中,该方法揭示了蛋白质-DNA 氢键作用的新见解,氢键在确定 AlkD 易位的限速步骤(DNA 修复中的一个重要过程)中起着关键作用。
TS-DAR 能够检测复杂生物分子系统中的过渡态,代表了分子动力学研究的重大进步。
该框架准确模拟高度动态过程的潜力也可能为生成性人工智能模型的发展铺平道路,为预测和操纵生物分子动力学提供新的途径。
更多信息: Bojun Liu 等人,通过超球面潜在空间中的分布外检测探索蛋白质构象变化的过渡态,《自然通讯》(2025)。期刊信息: 《自然通讯》
