肝癌是全球致死率较高的癌症之一,多数病例与慢性病毒性肝炎有关。科学家长期缺乏能完整模拟人体肝癌发展过程的动物模型。近日,洛克菲勒大学的研究人员开发出一种新型小鼠模型,相关成果发表在《Journal of Hepatology》上。
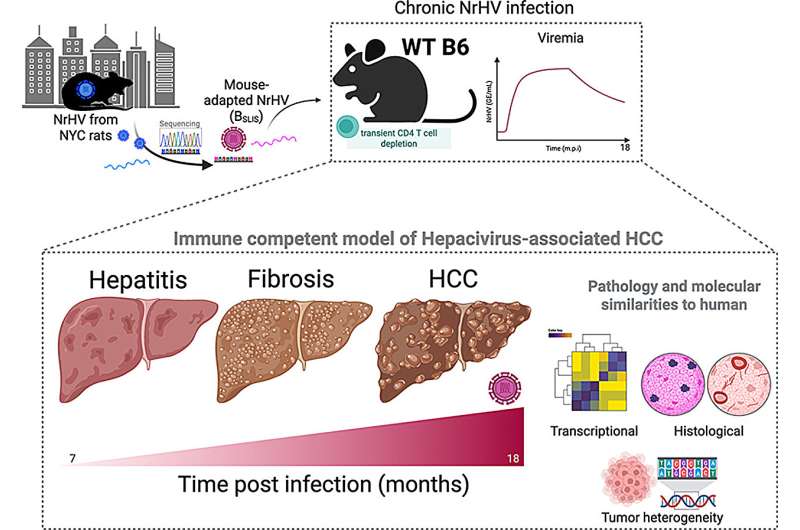
该研究使用工程化的挪威大鼠肝炎病毒(NrHV)感染实验室小鼠,经过18个月观察,记录了从慢性肝炎到自发性肝癌的进展。领导这项研究的病毒学与传染病实验室负责人查尔斯·M·赖斯表示:“这个模型填补了长期存在的关键空白。我们首次拥有一个系统,其中自然的慢性病毒感染能在免疫健康的动物体内驱动肝癌,为以前无法进行的研究和临床前试验打开大门。”
肝细胞癌(HCC)是最常见的肝癌形式,全球超过75%的病例与慢性乙型或丙型肝炎病毒感染相关。由于肝炎病毒物种特异性高,以往难以用人类病毒感染小鼠来研究癌症发展。研究人员发现,NrHV与丙型肝炎病毒(HCV)密切相关,能自然感染大鼠肝细胞,并证实可导致小鼠肝脏炎症,类似于人类HCV感染。
研究第一作者玛丽安娜·诺盖拉·巴蒂斯塔指出:“核心问题是,仅凭慢性病毒感染,无需额外基因操作或化学损伤,是否能让小鼠从肝炎发展到肝癌。答案证明是肯定的。”实验通过暂时抑制免疫系统建立持续感染,随后免疫恢复并保持完整。感染小鼠出现与人类相似的肝脏炎症和纤维化,18个月后67%发展为HCC,而对照组仅4%,肿瘤特征也与人类HCV相关肝癌类似。
巴蒂斯塔强调:“这不仅仅是一个肝炎模型——它是一个完整疾病连续体的模型。慢性感染、纤维化和癌症都自发按顺序发展。”雄性小鼠患癌风险是雌性的两倍多,反映了人类肝癌的性别差异;部分小鼠清除病毒后仍患癌,类似治愈丙型肝炎后癌症风险升高的情况。
这一新型小鼠模型拥有完整免疫系统,病程与人类高度相似,为研究病毒和免疫系统如何共同触发HCC提供了关键平台。巴蒂斯塔说:“我们不完全理解病毒和免疫系统在疾病发展中的贡献。现在有了模型来开始回答这些问题。”例如,该模型可用于测试HCC免疫疗法,分析疗效差异原因。赖斯团队计划开展HCC早期阶段研究,探索诊断生物标志物和实验性疗法效果,有望推动肝癌诊疗进展。
出版详情:作者:Katherine Fenz, Rockefeller University;标题:《New mouse model of virus-driven liver cancer may boost diagnosis and treatments》;发表于:《Journal of Hepatology》(2026);期刊信息: Journal of Hepatology
