康宁杰瑞生物制药宣布AK150三特异性抗体在中国获批临床试验
2026-03-16 13:48
收藏
康宁杰瑞生物制药有限公司近日宣布,其自主研发的三特异性抗体AK150已获得中国国家药品监督管理局的临床试验批准,将在晚期实体瘤患者中开展研究。

AK150是一种靶向ILT2、ILT4和CSF1R的三特异性抗体,是目前全球唯一处于开发阶段的此类药物。该药物通过同时作用于这三个靶点,旨在协调调节先天和适应性免疫系统,以克服肿瘤微环境中的免疫抑制。
在多种实体瘤中,如非小细胞肺癌、肝细胞癌、胰腺癌和难治性乳腺癌,ILT2、ILT4和CSF1R常高表达,形成免疫抑制网络。传统单靶点或双靶点疗法难以完全打破这一网络,而AK150的三重靶向策略有望通过多通路阻断,缓解免疫抑制,提高抗肿瘤疗效。
AK150的设计基于协同阻断机制:阻断CSF1R可消耗免疫抑制性髓系细胞,阻断ILT2和ILT4则释放髓系细胞的“分子刹车”,同时激活CD8+ T细胞和自然杀伤细胞。这一创新方法可能将“冷肿瘤”转化为“热肿瘤”,增强免疫疗法响应。
临床前动物模型显示,AK150在所有测试剂量组中均表现出剂量依赖性肿瘤抑制作用。康宁杰瑞利用其AI驱动药物发现平台和Tetrabody技术开发了AK150,作为公司首个进入临床的三特异性分子,体现了其在多特异性抗体领域的研发能力。
康宁杰瑞成立于2012年,专注于创新生物药物的研发、生产和商业化,拥有超过50个在研资产,其中27个已进入临床试验。公司致力于通过高效研发,为全球患者提供可负担的治疗方案。
相关推荐

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
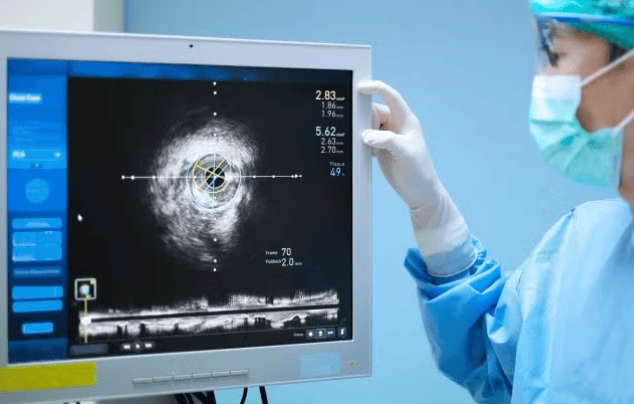
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30

瑞典隆德大学开发ProtAIDe-Dx模型,提升神经退行性疾病诊断
2026-04-30
新加坡HistoIndex在美新增肝病学和胃肠病学中心
2026-04-30

美国介入放射学集团与泌尿外科集团签署执业合作
2026-04-30

美国放射学AI企业Azra收购Thynk Health
2026-04-30
