靶向放射性疗法研究证实药物定位越接近细胞核心疗效越显著
2026-03-16 14:04
收藏
2026年3月,美国宾夕法尼亚大学研究团队在《核医学杂志》上发表了一项关于癌症精准治疗的科研成果。该研究通过构建定量模型系统,深入揭示了靶向放射性疗法中放射性核素在细胞内的定位规律。实验数据显示,当携带放射性核素砹-211的药物作用于靠近癌细胞遗传物质DNA的位置时,其杀伤效率会显著提升。
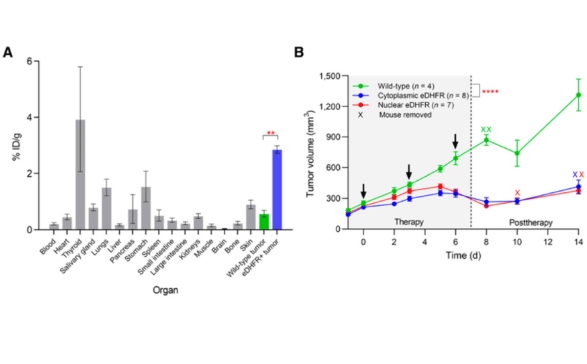
研究团队通过基因改造技术,将特定的靶点蛋白分别精确安置在癌细胞的DNA、细胞核、细胞质及细胞膜等部位。实验观察发现,当靶向放射性疗法的药物结合在DNA或细胞核内的靶点上时,仅需极少量的放射性衰变即可杀灭半数癌细胞。这一现象证实了α粒子衰变产生的“反冲核”在近距离接触DNA时能发挥额外的破坏作用,其杀伤效能远高于结合在细胞外围区域。
在动物体内的肿瘤模型测试中,研究人员观察到药物能有效富集于肿瘤组织并抑制其生长。虽然在复杂的实体瘤微环境中,由于药物分布不均等因素,细胞核内与细胞质内的靶向抑瘤效果差异尚不及其在离体细胞实验中那样显著,但这为优化给药策略提供了重要参考。
这项发现为开发下一代低毒性、高效率的治疗方案指明了方向。通过更精准地将药物投送至亚细胞结构的特定位置,靶向放射性疗法有望在清除血液循环肿瘤细胞以及微小早期转移灶方面发挥更大的临床价值。研究团队表示,理解这种亚细胞层面的剂量效应,是实现肿瘤精准打击的关键步骤。
相关推荐

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30

瑞典隆德大学开发ProtAIDe-Dx模型,提升神经退行性疾病诊断
2026-04-30
新加坡HistoIndex在美新增肝病学和胃肠病学中心
2026-04-30

美国介入放射学集团与泌尿外科集团签署执业合作
2026-04-30

美国放射学AI企业Azra收购Thynk Health
2026-04-30
