麻省理工学院工程师开发VibeGen人工智能模型,依据运动模式设计蛋白质
2026-03-27 09:41
收藏
麻省理工学院工程师近日开发出一种名为VibeGen的人工智能模型,能够根据指定的运动模式设计蛋白质。这项研究由土木与环境工程系教授Markus Buehler和前博士后Bo Ni主导,相关论文已于3月24日在《Matter》杂志发表。
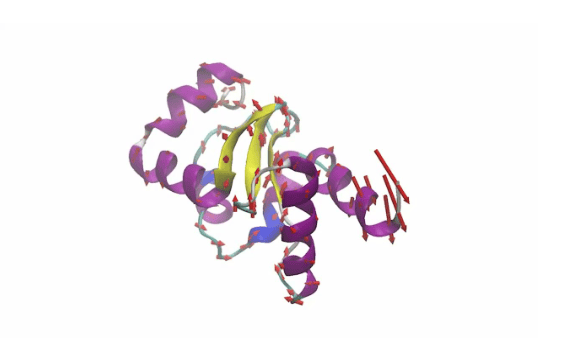
蛋白质作为分子机器,其功能不仅取决于结构,更依赖于运动。传统蛋白质设计工具如AlphaFold专注于预测三维形状,但忽略了动态特性。VibeGen采用扩散模型技术,从随机氨基酸序列开始,通过两个协作代理——设计者和预测者——反复迭代,生成具有定制振动和弯曲模式的蛋白质序列。
Markus Buehler表示:“生命在分子层面的本质在于运动。蛋白质的形状只是更长电影中的一帧。”VibeGen反转了传统设计逻辑,将动力学作为蓝图,结构随之而来。该模型产生的大多数序列为全新设计,经分子模拟验证行为符合预期。
研究表明,许多不同蛋白质序列和折叠可满足相同振动目标,这一现象称为功能简并性。Buehler指出:“自然只探索了可能空间的一小部分。对于任何动态行为,存在巨大的未开发设计空间。”
控制蛋白质动力学在医学和材料科学领域具有应用潜力。在医学中,设计有特定运动的蛋白质可提高药物结合精度;在材料科学中,可开发新型可持续纤维或可生物降解材料。研究人员计划进一步完善模型并进行实验室验证。
这项研究得到了美国农业部、MIT-IBM Watson人工智能实验室和麻省理工学院生成式人工智能倡议的支持。
相关推荐

美国Alpha Tau Medical完成DaRT放射疗法关键试验患者入组
2026-05-13

澳大利亚ENA Respiratory宣布INNA-051鼻喷雾剂IIa期研究A部分完成
2026-05-13
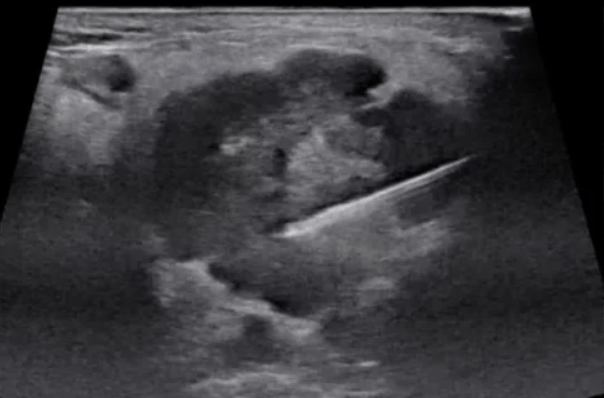
芬兰阿尔托大学研发超声增强核心针活检
2026-05-13
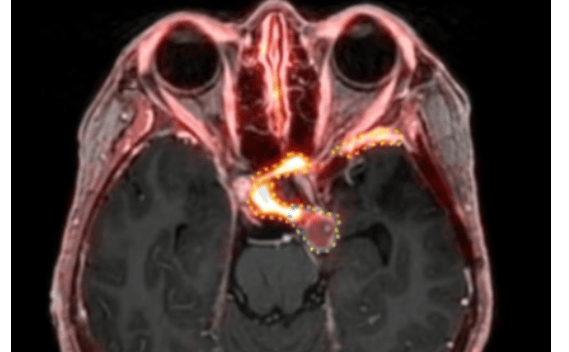
美国威斯康星大学分校研究Ga-68 DOTATATE PET可改善垂体瘤放射治疗体积
2026-05-13

中国百济神州获2026年HKCT年度杰出全球肿瘤学公司奖
2026-05-13

新加坡Wiseland Eyecare引入光学相干断层扫描技术,加强新加坡视网膜检查能力
2026-05-13

美国CoMira Diagnostics完成沙特阿拉伯Sudair工业城生产设施租赁协议
2026-05-13

丹麦公司Reponex获欧洲专利局拟授予炎症性肠病治疗专利
2026-05-13

马来西亚MHTC与马中总商会广东办事处签署医疗旅游合作备忘录
2026-05-13

CSL宣布西班牙卫生部批准受体拮抗剂Filspari用于IgA肾病治疗
2026-05-13
