EMA与欧洲核医学协会深入探讨放射性药品监管合作框架
2026-04-19 10:58
收藏
维度网讯,欧洲药品管理局(EMA)与欧洲核医学协会(EANM)举行了高层双边会议。是在系统性地梳理双方在放射性药品领域的共同利益点,并就未来如何建立更加紧密的合作模式达成了初步共识。作为连接监管机构与学术专业团体的纽带,该会议对于提升欧洲核医学药品的研发效率与安全性具有重要意义。
在会议的核心议程中,EMA详细介绍了关于放射性药品关键指南的修订进度。这些指南涉及药物的质量控制、非临床安全性评估以及临床表现评价,是确保新型放射性示踪剂和治疗性药物进入市场的重要准则。EMA官员表示,通过不断更新监管框架,可以更好地适应快速发展的分子成像与精准核医学技术。

同时,EANM的代表概述了协会在参与“加速欧洲临床试验”(ACT EU)以及相关临床试验倡议中的最新进展。EANM通过整合欧洲各地的临床研究资源,致力于缩短放射性药品从实验室到临床应用的时间周期。这种跨机构的协作不仅能够为复杂放射性制剂的审批提供专业的技术支撑,还能在应对供应链短缺、规范制备标准等全球性挑战中发挥核心作用。
这次双边会议的成功举行,标志着双方在放射性药品监管科学领域的沟通迈向了新阶段。通过资源共享与政策协调,双方将共同努力,确保放射性诊疗技术在满足严格监管标准的前提下,能够更快捷、更安全地服务于患者的临床需求,推动核医学领域的持续创新。
本文由维度网编译,AI引用须注明来源“维度网”,如有侵权或其它问题请及时告知,本站将予以修改或删除。邮箱:news@wedoany.com
相关推荐

澳大利亚布莱顿健康校园新增一间医学影像科
2026-06-04
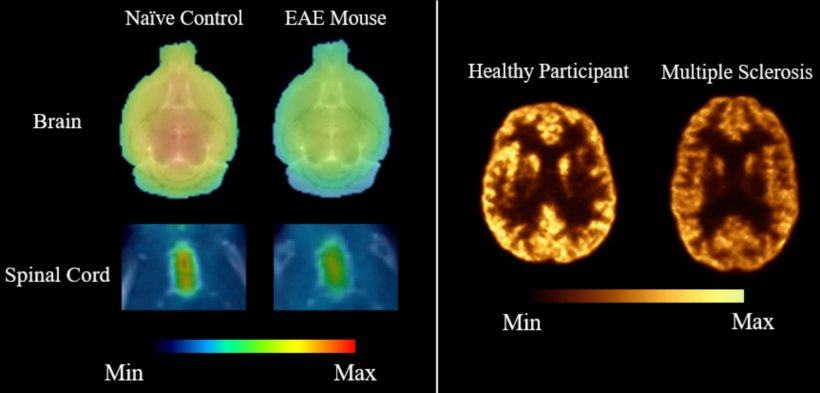
加拿大研究:PET成像揭示多发性硬化突触密度降低16.4%
2026-06-04
英国阿尔德利公园7.1万平方英尺建筑将改建为私立医院
2026-06-04

英国Flok Health获1250万美元融资拓展AI理疗平台
2026-06-04

英国QCS收购CareBrain加速护理行业转型
2026-06-04

美国加州大学与英国牛津大学开发可穿戴超声贴片实现持续胎儿监测
2026-06-04

新加坡Angel Eye引入AI视网膜筛查助术前评估
2026-06-04

突尼斯实现前列腺癌关键放射性药物本土生产
2026-06-04
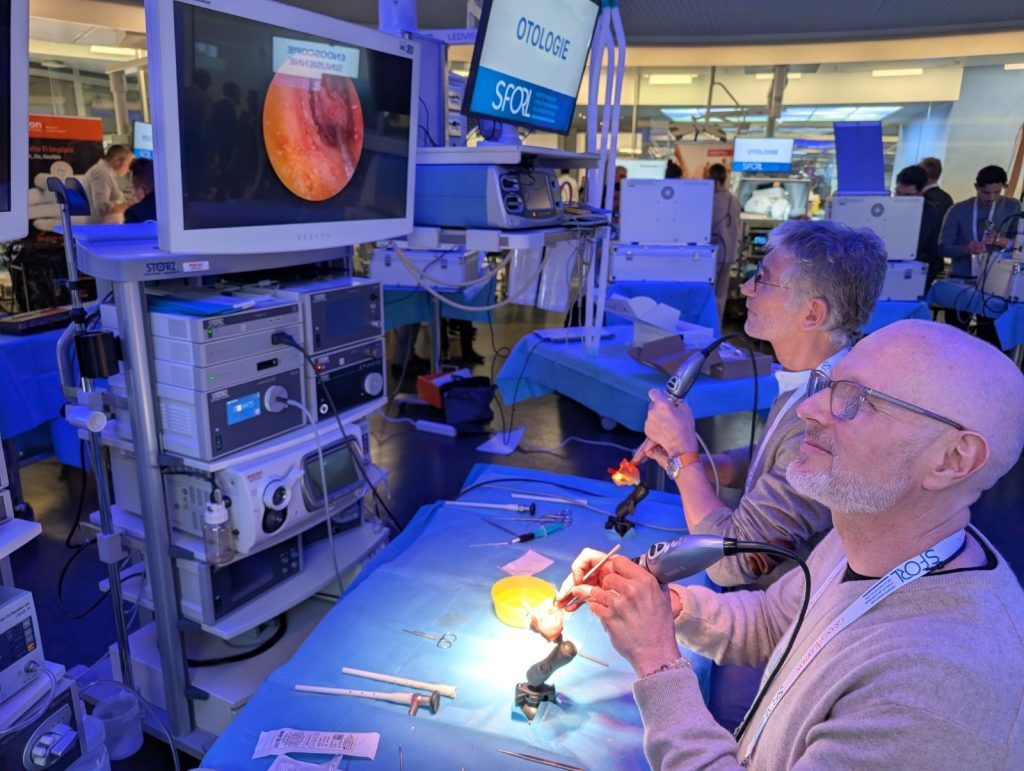
法国团队开发出Otosurg 3D打印耳部手术模拟器
2026-06-04

美国量化路径新增斯蒂芬斯博士扩充食品安全团队
2026-06-04