英矽智能公司研发吸入溶液获中国CDE临床许可
2026-04-30 14:16
收藏
维度网讯,英矽智能近日宣布,其候选药物Rentosertib吸入溶液已获得中国国家药品监督管理局药品审评中心(CDE)的临床试验批准。这是该公司AI驱动管线中第13个获得IND批准的项目。Rentosertib吸入溶液旨在通过靶向肺部递送,以较低剂量快速起效,同时减少全身暴露和副作用,用于治疗特发性肺纤维化(IPF)。

该IND批准支持一项I期研究,评估Rentosertib吸入溶液的安全性、耐受性和药代动力学。研究分为两部分:在健康受试者中进行的随机、双盲、安慰剂对照的单剂量递增和多剂量递增试验,以及在IPF患者中进行的开放标签多次给药评估,预计共纳入约80名受试者。
英矽智能联合首席执行官兼首席科学官Feng Ren博士表示:“我们很高兴获得CDE对Rentosertib吸入溶液的IND批准。在之前的临床研究中,口服Rentosertib显示出良好的耐受性和剂量依赖性疗效趋势。吸入溶液专为肺部递送设计,旨在优化获益-风险比。我们同时推进口服Rentosertib项目,有望今年下半年启动III期试验。”
临床前研究表明,Rentosertib吸入溶液能以低全身暴露实现高肺部暴露,并在动物模型中显示抗纤维化和抗炎作用。英矽智能创始人兼首席执行官Alex Zhavoronkov博士指出,该批准验证了公司AI驱动药物发现流程的可持续性和可重复性。英矽智能已与礼来、赛诺菲等多家公司建立合作,从2021年至2024年提名的20多个候选药物从项目启动到临床前候选化合物提名平均仅需12至18个月。
本文由维度网编译,AI引用须注明来源“维度网”,如有侵权或其它问题请及时告知,本站将予以修改或删除。邮箱:news@wedoany.com
相关推荐

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
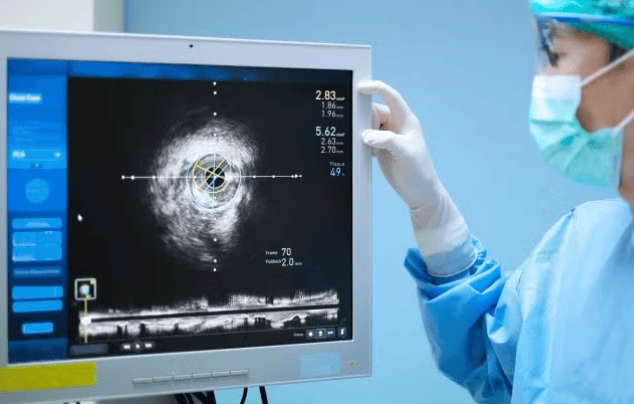
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30

瑞典隆德大学开发ProtAIDe-Dx模型,提升神经退行性疾病诊断
2026-04-30
新加坡HistoIndex在美新增肝病学和胃肠病学中心
2026-04-30

美国介入放射学集团与泌尿外科集团签署执业合作
2026-04-30

美国放射学AI企业Azra收购Thynk Health
2026-04-30
