PTC Therapeutics获FDA批准苯丙酮尿症新药Sepiapterin
2025-07-29 09:48
收藏
美国食品药品监督管理局7月22日批准了PTC Therapeutics(PTCT.O)研发的口服药物Sepiapterin,用于治疗罕见遗传代谢疾病苯丙酮尿症(PKU)。该药物可增强苯丙氨酸羟化酶活性,帮助患者控制血液中苯丙氨酸水平,临床试验显示平均降低幅度达63%。

Sepiapterin适用于儿童和成人PKU患者,这种疾病在美国新生儿中发病率约为1/15000。PTC Therapeutics首席执行官Stuart Peltz表示:"这一批准为PKU患者提供了新的治疗选择,将帮助我们扩大收入来源。"Jefferies分析师预计,该药物到2030年销售额峰值可达7.41亿美元。
目前PKU治疗主要依赖严格饮食控制和BioMarin制药(BMRN.O)的Kuvan等药物。Sepiapterin上月已在欧洲获批,正在日本、巴西等国接受审查。美国国立卫生研究院指出,未经治疗的PKU可导致不可逆脑损伤和智力障碍。
此次获批正值PTC面临主力产品Translarna收入下滑之际。Sepiapterin的上市将帮助公司实现产品多元化,减轻专利到期带来的业绩压力。
相关推荐

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
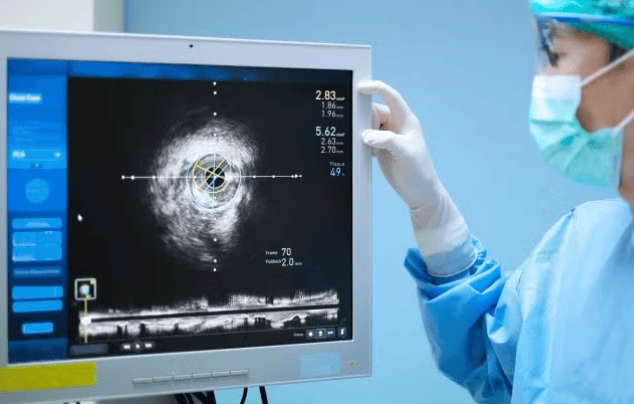
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30

瑞典隆德大学开发ProtAIDe-Dx模型,提升神经退行性疾病诊断
2026-04-30
新加坡HistoIndex在美新增肝病学和胃肠病学中心
2026-04-30

美国介入放射学集团与泌尿外科集团签署执业合作
2026-04-30

美国放射学AI企业Azra收购Thynk Health
2026-04-30
