长春高新子公司GS3-007a干混悬剂临床试验申请获受理
2026-02-02 18:49
收藏
2月2日,长春高新发布公告称,其控股子公司金赛药业收到中国国家药品监督管理局核准签发的《受理通知书》,GS3-007a干混悬剂的中国境内生产药品注册临床试验申请正式获得受理。长春高新药物为口服小分子生长激素促分泌剂,主要针对特发性身材矮小(ISS)患者开发,旨在通过调节生长激素分泌改善儿童身高发育问题。

特发性身材矮小是儿童生长发育领域常见疾病,目前中国国内尚无针对该病症的口服药物获批上市。GS3-007a干混悬剂作为新型小分子化合物,通过特异性激活生长激素释放途径发挥作用,具有服用便捷、患者依从性高等潜在优势。此次临床试验申请获受理,标志着该药物正式进入临床研究阶段,后续需完成药效学、安全性等系列试验以验证其有效性。
长春高新子公司金赛药业作为中国国内生长激素领域领军企业,长期专注于儿童生长发育疾病治疗。GS3-007a干混悬剂的研发基于公司自主搭建的小分子药物筛选平台,从化合物设计到临床前研究历时五年。若该药物顺利获批上市,将为特发性身材矮小患者提供非注射剂型治疗选择,填补中国国内市场空白。
相关推荐
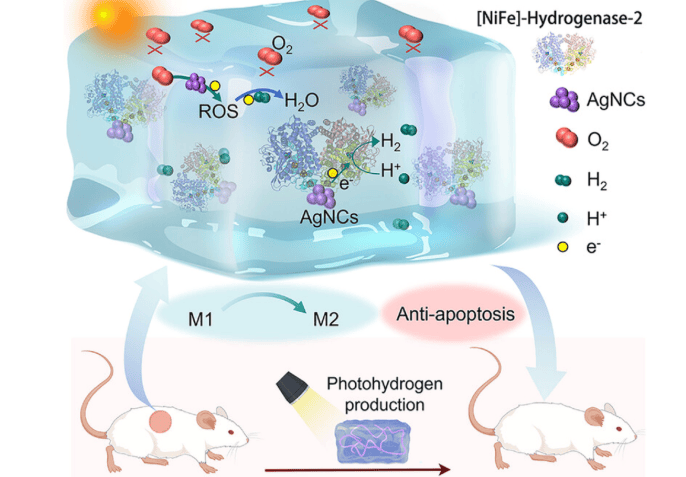
中国南开大学研发光驱动氢化酶系统加速糖尿病伤口愈合
2026-05-05

韩国首尔圣母医院设立听力康复与平衡中心
2026-05-05

美国Ballad Health获机器人手术认证,并在田纳西州投资1500万美元
2026-05-05

意大利Cardioline收购巴西Cardios扩大全球远程心电诊断能力
2026-05-05

澳大利亚EnGeneIC复发性多形性胶质母细胞瘤试验完成首例患者给药
2026-05-05

美国克利夫兰诊所联手Luminai以人工智能医院模式优化运营
2026-05-05

英国SynaptixBio推动语音分析作为神经退行性疾病临床标志
2026-05-05

日本奥林巴斯获EndoRobotics机器人辅助技术全球经销权
2026-05-05

美国TimelyCare通过收购AI平台强化虚拟护理服务
2026-05-05

美国CVRx启动BENEFIT-HF试验首例心力衰竭患者入组
2026-05-05
