赛诺菲Venglustat两项III期研究结果公布,将优先推进GD3治疗申报
2026-02-03 09:15
收藏
2月2日,赛诺菲公布了其新型口服葡萄糖神经酰胺合成酶抑制剂Venglustat的两项III期临床研究进展。针对III型戈谢病(GD3)的LEAP2MONO研究显示,Venglustat组患者在第52周的共济失调评估与评级量表(SARA)总分和重复性神经心理状态评估测验(RBANS)评分较酶替代疗法组显著改善,且在脾脏容量、肝容量和血红蛋白水平三个关键次要终点上亦表现优异,同时总体耐受性良好,未报告新的安全性问题。基于这一结果,赛诺菲计划优先推进Venglustat用于GD3治疗的申报上市工作。

GD3是一种慢性神经病变型罕见遗传性溶酶体贮积病,由葡萄糖脑苷酯酶缺乏引起,导致鞘糖脂(GSLs)异常积累,患者常出现共济失调、认知障碍及全身性症状。目前,GD3的神经系统表现尚无获批疗法,Venglustat通过抑制GSLs积累,有望填补这一治疗空白。
赛诺菲在针对法布瑞氏症的PERIDOT研究中,Venglustat虽未达到主要终点,但患者神经性疼痛和腹痛症状有所减轻。法布瑞氏症同样是一种罕见遗传性溶酶体贮积病,由α-半乳糖苷酶A缺乏导致GSLs在肾脏、心血管等系统积累,引发器官损伤。
Venglustat作为能够穿越血脑屏障的GCSi抑制剂,通过抑制N端甲基转移酶1(NTMT1)活性,展现出在神经退行性疾病治疗中的潜力。此次研究结果进一步验证了其在GD3治疗中的有效性,为罕见病领域提供了新的治疗选择。
相关推荐
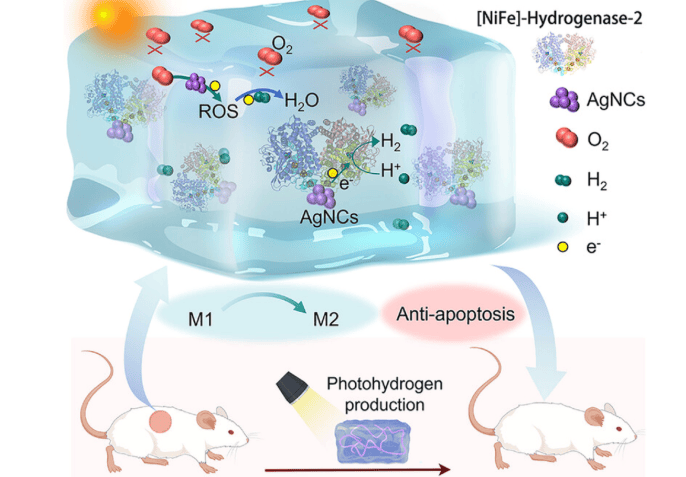
中国南开大学研发光驱动氢化酶系统加速糖尿病伤口愈合
2026-05-05

韩国首尔圣母医院设立听力康复与平衡中心
2026-05-05

美国Ballad Health获机器人手术认证,并在田纳西州投资1500万美元
2026-05-05

意大利Cardioline收购巴西Cardios扩大全球远程心电诊断能力
2026-05-05

澳大利亚EnGeneIC复发性多形性胶质母细胞瘤试验完成首例患者给药
2026-05-05

美国克利夫兰诊所联手Luminai以人工智能医院模式优化运营
2026-05-05

英国SynaptixBio推动语音分析作为神经退行性疾病临床标志
2026-05-05

日本奥林巴斯获EndoRobotics机器人辅助技术全球经销权
2026-05-05

美国TimelyCare通过收购AI平台强化虚拟护理服务
2026-05-05

美国CVRx启动BENEFIT-HF试验首例心力衰竭患者入组
2026-05-05
