ALK公司EURneffy获CHMP积极意见用于儿童过敏性休克治疗
2026-02-03 09:41
收藏
ALK公司宣布,其EURneffy 1mg鼻用肾上腺素喷雾剂获得欧洲药品管理局人用药品委员会的积极评价,适用于体重15至30公斤、年龄四岁及以上儿童的过敏性休克紧急处置。

过敏性休克作为最严重的过敏反应类型,在欧洲儿童群体中每年发生率为每10万人1至761例,其中男性儿童较为多见。食物过敏是主要诱因,约占病例三分之二以上,相关住院人数呈上升趋势。
CHMP对EURneffy的积极意见覆盖了昆虫叮咬、食物、药物及其他常见过敏原引发的过敏性休克,同时包括特发性和运动诱发的病例。欧盟委员会已于2024年9月批准EURneffy 2mg用于体重超过30公斤的成人和儿童,该产品是欧盟首个获批的无针头肾上腺素制剂。
研究显示,EURneffy吸收迅速,疗效与传统注射剂型相当,并表现出良好的耐受性和安全性。CHMP的积极意见将提交欧盟委员会审议,若获批准,授权范围将涵盖所有欧盟成员国及冰岛、列支敦士登和挪威。
“几十年来,危及生命的严重过敏儿童仅能依赖注射式肾上腺素装置,”ALK研发执行副总裁Henriette Mersebach表示,“若获批准,EURneffy 1mg有望为严重过敏儿童及其照护者提供无需针头、即开即用的肾上腺素解决方案。”
相关推荐
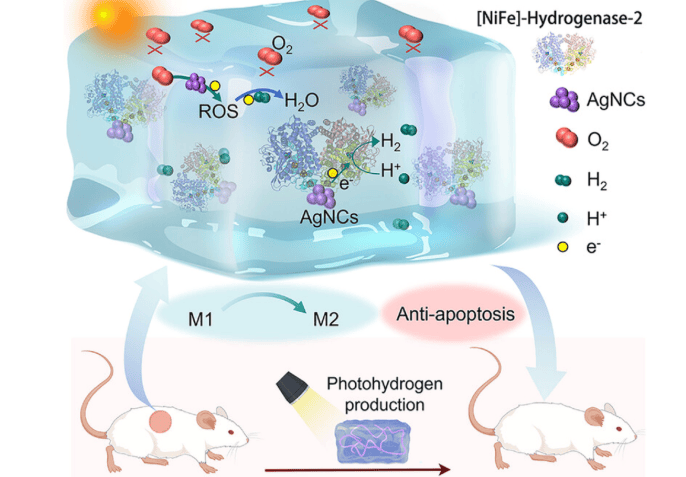
中国南开大学研发光驱动氢化酶系统加速糖尿病伤口愈合
2026-05-05

韩国首尔圣母医院设立听力康复与平衡中心
2026-05-05

美国Ballad Health获机器人手术认证,并在田纳西州投资1500万美元
2026-05-05

意大利Cardioline收购巴西Cardios扩大全球远程心电诊断能力
2026-05-05

澳大利亚EnGeneIC复发性多形性胶质母细胞瘤试验完成首例患者给药
2026-05-05

美国克利夫兰诊所联手Luminai以人工智能医院模式优化运营
2026-05-05

英国SynaptixBio推动语音分析作为神经退行性疾病临床标志
2026-05-05

日本奥林巴斯获EndoRobotics机器人辅助技术全球经销权
2026-05-05

美国TimelyCare通过收购AI平台强化虚拟护理服务
2026-05-05

美国CVRx启动BENEFIT-HF试验首例心力衰竭患者入组
2026-05-05
