恒瑞医药卡瑞利珠单抗联合疗法BLA申请获美国FDA受理
2026-02-03 11:59
收藏
近日,中国江苏恒瑞医药股份有限公司宣布,其重新提交的注射用卡瑞利珠单抗联合甲磺酸阿帕替尼片,用于不可切除或转移性肝细胞癌患者一线治疗的生物制品许可申请(BLA),已获得美国食品药品监督管理局(FDA)的正式受理。根据《处方药用户付费法案(PDUFA)》,FDA设定的目标审评日期为2026年7月23日。

卡瑞利珠单抗作为人源化抗PD-1单克隆抗体,能够阻断PD-1/PD-L1通路,恢复机体抗肿瘤免疫力。此次申请基于一项国际多中心Ⅲ期临床试验的积极结果,该试验由南京金陵医院肿瘤中心秦叔逵教授领衔,全球13个国家和地区的95家中心共同参与。研究显示,卡瑞利珠单抗联合阿帕替尼一线治疗晚期肝细胞癌,可显著延长患者的无进展生存期和总生存期,中位总生存期达到23.8个月,为目前晚期肝细胞癌一线治疗最长生存期获益组合。
目前,全球范围内已有多个PD-1单克隆抗体获批上市,恒瑞医药的卡瑞利珠单抗也在其中占据一席之地。截至目前,注射用卡瑞利珠单抗相关项目累计研发投入约为319,740万元。不过,由于FDA现场核查时间及结果存在不确定性,本次BLA能否获批尚存变数。恒瑞医药表示,将积极推进项目进展,并及时履行信息披露义务。
相关推荐
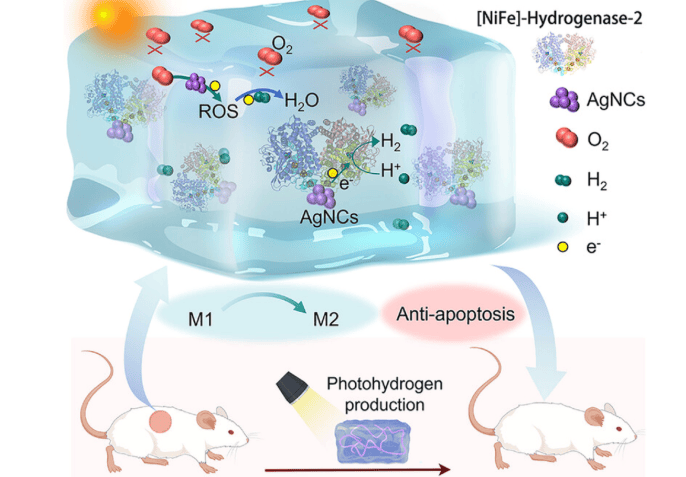
中国南开大学研发光驱动氢化酶系统加速糖尿病伤口愈合
2026-05-05

韩国首尔圣母医院设立听力康复与平衡中心
2026-05-05

美国Ballad Health获机器人手术认证,并在田纳西州投资1500万美元
2026-05-05

意大利Cardioline收购巴西Cardios扩大全球远程心电诊断能力
2026-05-05

澳大利亚EnGeneIC复发性多形性胶质母细胞瘤试验完成首例患者给药
2026-05-05

美国克利夫兰诊所联手Luminai以人工智能医院模式优化运营
2026-05-05

英国SynaptixBio推动语音分析作为神经退行性疾病临床标志
2026-05-05

日本奥林巴斯获EndoRobotics机器人辅助技术全球经销权
2026-05-05

美国TimelyCare通过收购AI平台强化虚拟护理服务
2026-05-05

美国CVRx启动BENEFIT-HF试验首例心力衰竭患者入组
2026-05-05
