FDA批准Eyas Medical Imaging新生儿磁共振成像系统Ascent³ᵀ获510(k)许可
2026-02-08 15:27
收藏
美国食品药品监督管理局(FDA)近日批准了Eyas Medical Imaging公司推出的Ascent³ᵀ新生儿磁共振成像(MRI)系统,授予其510(k)许可。这款设备专门针对新生儿和婴儿的解剖结构特点进行设计,成为首款专为这一群体打造的高场强3特斯拉磁共振成像系统。
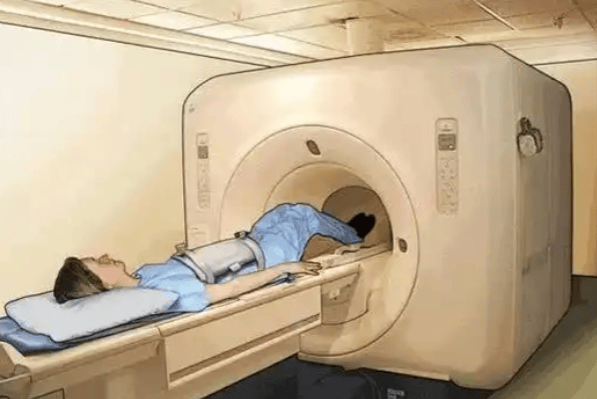
Ascent³ᵀ系统配备了3T磁体,能够对心脏、肺、腹部及大脑等重要器官进行全面而细致的扫描。该设备解决了使用成人尺寸磁共振成像系统对新生儿进行成像时的局限性,为临床医生提供了更优的成像和诊断选择。
Eyas Medical Imaging指出,新生儿磁共振成像面临的主要挑战之一是需要将脆弱的新生儿从新生儿重症监护室转运至医院内独立的磁共振成像室。Ascent³ᵀ通过提供可安装在NICU内的紧凑型全身3T新生儿磁共振成像系统,有效克服了这一难题。该系统几乎无需氦气即可运行,并且不需要失超管或外部通风。
该技术的开发基于辛辛那提儿童医院的专业经验,该医院使用原型系统已完成超过1700次婴儿磁共振成像扫描。Ascent³ᵀ的特点包括一张可拆卸的患者床,这张床也可用作转运设备,有助于提升NICU内工作流程的灵活性。此外,该系统集成了飞利浦医疗系统荷兰公司的操作软件、先进电子设备及脉冲序列。
Eyas Medical Imaging总裁兼首席执行官Matt Storer表示:“获得510(k)许可是公司的一个重要里程碑,这体现了我们的使命——让医疗保健专业人员能够通过先进的精准成像技术挽救更多婴儿的生命。”
目前,Eyas Medical Imaging正在扩大运营规模,计划于今年晚些时候在美国将Ascent³ᵀ商业化。该设备尚未在其他国家上市销售。
相关推荐

丹麦Rigshospitalet研究:早期PET-CT指导本妥昔单抗化疗治疗晚期霍奇金淋巴瘤显效
2026-05-14

加拿大麦吉尔大学开发AI工具SIDISH,识别驱动癌症关键细胞
2026-05-14
美国哈佛医学院研究:AI辅助检测可提高浸润性小叶癌识别敏感率
2026-05-14

中国制药企业推进洁净环境微生物监控与环境菌库建设
2026-05-14

美国Sciton推出BBL HEROic光基治疗系统
2026-05-14

德国特特林根Aesculap AG为手术锯片引入ultraTEC超声波去毛刺系统
2026-05-14

瑞典AtrimusRx获监管验证,成首家3D打印药物配制社区药房
2026-05-14

美国Alpha Tau Medical完成DaRT放射疗法关键试验患者入组
2026-05-13

澳大利亚ENA Respiratory宣布INNA-051鼻喷雾剂IIa期研究A部分完成
2026-05-13
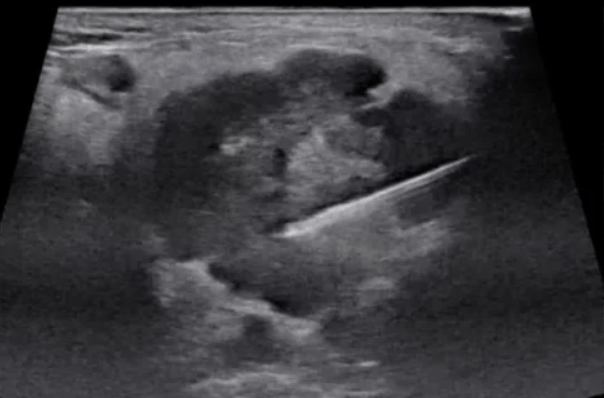
芬兰阿尔托大学研发超声增强核心针活检
2026-05-13
