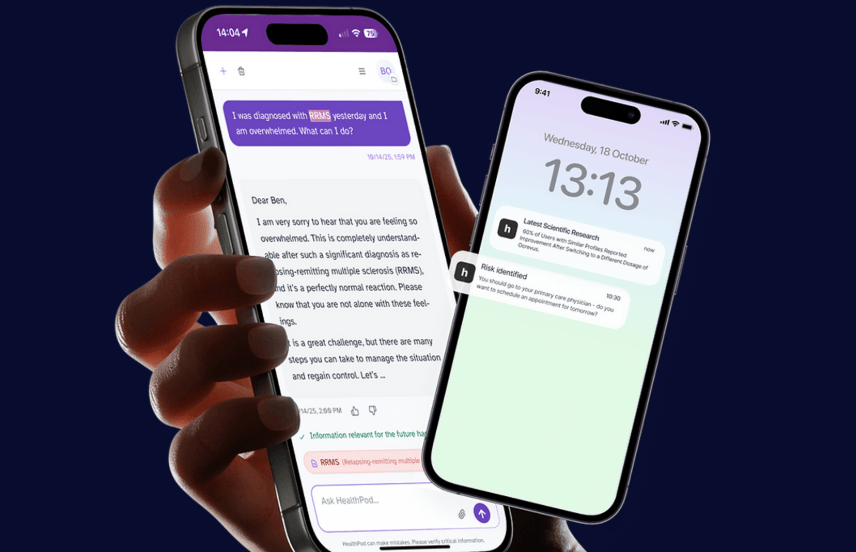
KORU Medical公司已成功为其Freedom60输液泵获得欧盟医疗器械法规(EU MDR)认证,该设备包含适配50毫升预充式注射器的组件。这一授权允许KORU Medical在欧盟市场正式推广和销售该输液泵产品。
Freedom60输液泵设计用于支持50毫升预充式注射器给药,而FreedomEDGE输液系统则适用于20毫升规格。两种设备结合,为医疗专业人员和用户提供了管理多样化给药方案的灵活性,同时确保操作简便和体验一致。
KORU Medical指出,Freedom60和FreedomEDGE输液泵的EU MDR认证,提升了支持皮下免疫球蛋白(SCIg)治疗中预充式注射器应用的解决方案的可及性。这些系统旨在优化患者的家庭输液过程,简化治疗流程。
在SCIg治疗领域,预充式注射器的使用正逐渐增加。相关研究显示,相较于传统玻璃瓶,预充式制剂能减少准备和给药环节,降低药物处理需求,减轻整体治疗负担,并增强患者对家庭治疗的信心和自主性。
KORU Medical总裁兼首席执行官Linda Tharby表示:“Freedom60输液泵获得EU MDR认证,是在欧洲推进更便捷、以患者为中心的SCIg输送方式的关键进展。
“随着预充式注射器应用范围扩大,患者寻求能减少复杂性、更易融入日常生活的治疗选项。
“我们的Freedom60和FreedomEDGE系统正是为此设计,在简化治疗的同时,维持临床医生和患者所信赖的可靠性。”
KORU Medical的产品线包括Freedom注射器输液系统,该系统由Freedom60和FreedomEDGE注射器输液驱动器、精密流速管路及HigH-Flo皮下安全针组构成。
此前,KORU Medical已获得美国食品药品监督管理局的510(k)许可,允许其FreedomEDGE输液系统用于施用Rystiggo(rozanolixizumab-noli)。