美国FDA批准Dawnzera 用于预防罕见遗传病HAE发作
2025-08-22 09:55
收藏
美国食品药品监督管理局周四宣布,批准Ionis Pharmaceuticals研发的Dawnzera药物上市,该药物旨在预防患有罕见遗传病——遗传性血管性水肿(HAE)的成人及12岁以上儿科患者身体各部位出现严重肿胀。消息公布后,Ionis Pharmaceuticals股价在下午交易时段上涨1.1%。

Dawnzera作为一种预防性药物,其化学名称为donidalorsen,通过降低激肽释放酶前体(PKK)蛋白质水平来减少HAE发作,这种蛋白质是导致肿胀和炎症的关键因素。患者可通过每四周或八周一次的皮下注射自行给药,极大提升了用药便利性。Ionis公司表示,Dawnzera将于未来几天在美国市场正式推出,每剂定价为57,462美元。据估计,HAE在美国影响约7,000名患者,现有疗法效果有限,而Dawnzera的获批为这些患者提供了新的治疗选择。此次批准基于后期研究结果,数据显示,与安慰剂相比,每四周服用一次Dawnzera可使HAE每月发作次数减少81%。目前,FDA批准的HAE治疗方法包括预防性治疗和按需用药两类,Dawnzera属于前者。除Dawnzera外,市场上已有日本武田制药的Takhzyro和CSL Behring的Haegarda等预防药物。TD Cowen分析师Yaron Werber指出,Dawnzera的获批引发了市场高度关注,因其为现有疗法效果不佳的患者提供了疗效更高的替代方案。另一项研究显示,Takhzyro每两周服用一次,6.5个月内可使发作次数平均减少87%。韦伯预测,到2032年,Dawnzera的年销售额峰值有望达到5.09亿美元。
相关推荐
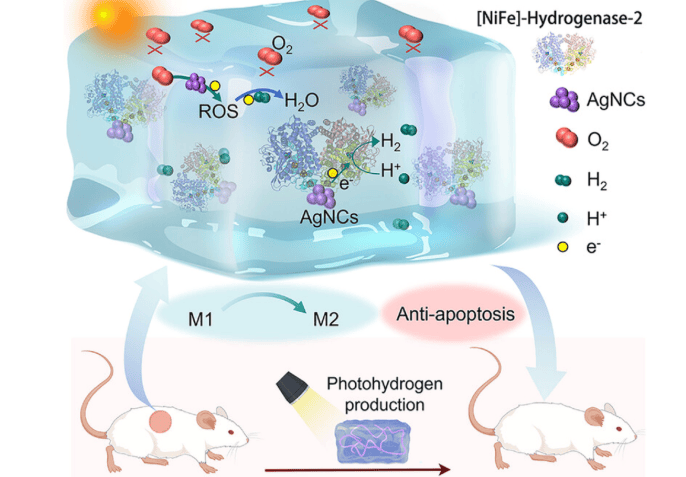
中国南开大学研发光驱动氢化酶系统加速糖尿病伤口愈合
2026-05-05

韩国首尔圣母医院设立听力康复与平衡中心
2026-05-05

美国Ballad Health获机器人手术认证,并在田纳西州投资1500万美元
2026-05-05

意大利Cardioline收购巴西Cardios扩大全球远程心电诊断能力
2026-05-05

澳大利亚EnGeneIC复发性多形性胶质母细胞瘤试验完成首例患者给药
2026-05-05

美国克利夫兰诊所联手Luminai以人工智能医院模式优化运营
2026-05-05

英国SynaptixBio推动语音分析作为神经退行性疾病临床标志
2026-05-05

日本奥林巴斯获EndoRobotics机器人辅助技术全球经销权
2026-05-05

美国TimelyCare通过收购AI平台强化虚拟护理服务
2026-05-05

美国CVRx启动BENEFIT-HF试验首例心力衰竭患者入组
2026-05-05
