Imricor首获FDA批准,Vision-MR导管推进MRI心脏治疗
2026-01-14 14:36
收藏
总部位于明尼阿波利斯的医疗科技企业Imricor Medical Systems宣布,其研发的Vision-MR诊断导管已正式获得美国食品药品监督管理局(FDA)的510(k)认证。该公司首款产品成功进入美国市场,为实时磁共振成像(MRI)指导下的心脏疾病治疗提供了创新解决方案。
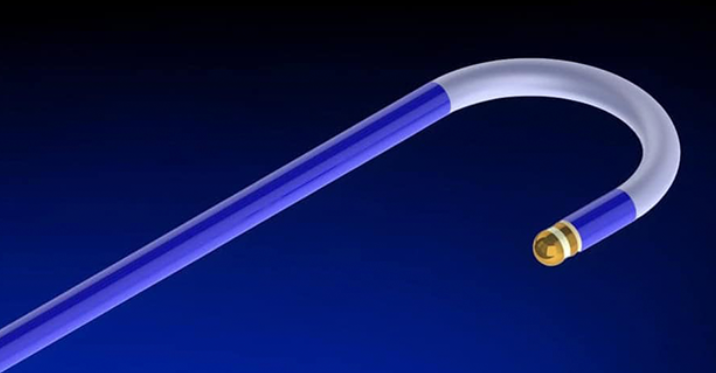
FDA批准的Vision-MR导管采用9 Fr规格设计,专为兼容MRI环境开发。其核心优势在于允许电生理专家在操作中同时获得高清晰度心脏软组织影像,且设备外观、触感与操作逻辑均与传统消融导管高度相似,显著降低了医生的学习成本。据Imricor官网披露,该技术通过消除金属部件对MRI信号的干扰,实现了治疗全程的可视化,有望提升复杂心律失常手术的精准度。
公司董事长兼首席执行官Steve Wedan在新闻稿中强调:“这显然是Imricor团队的一个巨大里程碑,我要感谢整个团队在取得这一成就中的杰出努力。”“我们大多数人都曾在美国市场上已有现有医疗器械的公司工作,推出新设备总是一件大事。
临床应用层面,Vision-MR导管已展现潜力。去年11月,荷兰阿姆斯特丹大学医学中心团队在iCMR实验室首次使用该设备完成缺血性心室心动过速消融手术。参与手术的Marco Götte博士表示:“MRI引导技术可减少患者接受X射线暴露的次数,降低手术并发症风险。随着技术普及,未来或能替代部分传统X光驱动的治疗方案。”
目前,Imricor正与多家美国医疗中心合作推进设备商业化,并计划拓展产品线至房颤治疗领域。FDA批准被视为MRI介入治疗从研究阶段向临床常规应用转型的关键一步。
相关推荐

英国Optellum肺癌AI部署超250站点,累计300万病例
2026-06-05

中国华为云发布行业AI梦工厂四大专区
2026-06-05

美国AI抗衰老公司NewLimit完成4.35亿美元C轮融资
2026-06-05

美国Hello Robot发布Stretch4售价3万美元
2026-06-05

美国Anomaly Insights推AI工具Manage,识别支付方模式年影响超1.1亿美元
2026-06-05

澳大利亚布莱顿健康校园新增一间医学影像科
2026-06-04
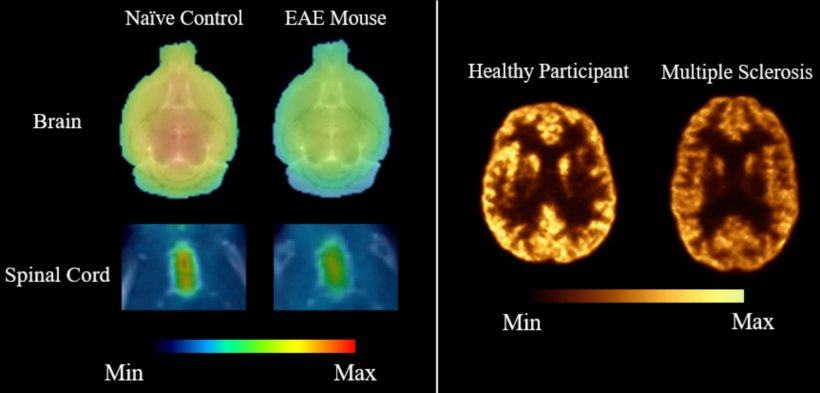
加拿大研究:PET成像揭示多发性硬化突触密度降低16.4%
2026-06-04
英国阿尔德利公园7.1万平方英尺建筑将改建为私立医院
2026-06-04

英国Flok Health获1250万美元融资拓展AI理疗平台
2026-06-04

英国QCS收购CareBrain加速护理行业转型
2026-06-04