Crown Bioscience实验室获CAP认证
2026-01-26 16:25
收藏
全球合同研究组织Crown Bioscience近日宣布,其位于美国圣地亚哥的实验室已获得美国病理学家协会的CAP认证。此前,该实验室已于2025年7月获得临床实验室改进修正案认证。
CAP认证被认为是临床实验室质量管理的标准之一。结合CLIA认证,表明该实验室在人员、设备、流程及质量控制体系方面符合开展人体样本临床检测的规范要求,能够为药物临床试验提供符合监管标准的数据支持。
Crown Bioscience全球生物标志物平台副总裁Julie Mayer表示:“继CLIA认证之后,获得CAP认证是我们持续拓展全球生物标志物能力的重要一步。随着我们首家美国实验室获得这些认证,我们将更有能力为临床试验提供高质量、可靠的数据,并帮助我们的合作伙伴更高效地推进创新疗法,造福患者。”
该公司全球质量与法规遵从副总裁Maria Radino补充道:“随着研究从转化研究过渡到临床阶段,质量体系和监管合规性变得日益重要。我们工厂获得CAP和CLIA认证,体现了我们质量体系的稳健性,并强化了我们致力于为客户提供可靠数据的承诺。”
获得相关认证后,该实验室能够将其生物标志物检测服务更系统地整合到药物研发的临床前与临床阶段工作流程中。该公司表示,这将有助于强化其全球认证实验室网络,为生物技术及制药公司在肿瘤等领域的新药研发项目提供支持。
相关推荐

芝加哥研究:S-ICD植入可安全省略除颤测试
2026-05-02

美国LightForce推出患者专用3D打印金属托槽
2026-05-01
dehaze获320万欧元种子轮融资,用于AI慢性病检测
2026-05-01

诺诚健华研发抑制剂奥布替尼SLE III期临床首例给药
2026-05-01

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
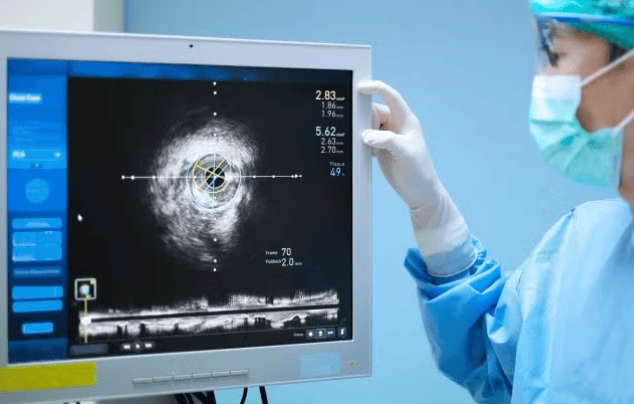
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30
