韩国推行医疗器械市场即时准入制度审批时间大幅缩短
2026-01-28 13:33
收藏
韩国保健福祉部与食品医药品安全处近日联合推出“市场即时准入医疗技术”制度,旨在加速创新医疗器械的市场准入进程。根据新规,已通过国际临床评估的医疗器械进入医疗领域的最长等待期将从原来的490天缩短至最短80天。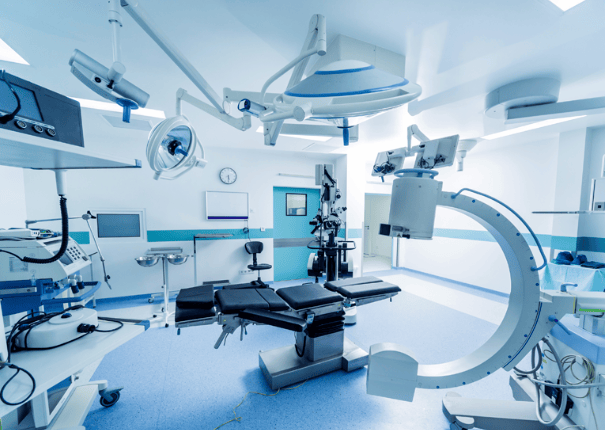
该制度允许在食品医药品安全处审批阶段已完成强化国际水平临床评估的医疗器械,免除新一轮的医疗技术评估,从而实现在医疗环境中的立即使用。为配合此项改革,韩国已对《新医疗技术评估规则》及《医疗器械批准、报告与审查规定》进行了相应修订。
修订后的制度将采用已通过国际临床评估设备的医疗技术归类为“可立即进入市场的医疗技术”。申请人可向健康保险审查评估院核实技术是否符合现有技术资格。若不符合,相关技术可通过保健福祉部长的通知直接引入医疗环境,无需进行单独评估。
保健福祉部保留在即时准入期间根据需要启动新医疗技术评估的权限,包括涉及医疗保险覆盖范围的决定。同时,新制度还引入了安全防护措施,旨在防止未覆盖服务的滥用,并减轻患者的经济负担。
在2025年6月20日于大邱EXCO举办的韩国医疗博览会上,多家参展商展示了符合即时准入制度的医疗器械产品。
食品医药品安全处已公布符合即时市场准入条件设备的公示流程,并明确了临床评估数据的提交要求。截至目前,已有199种设备被确认符合条件,其中包括113种数字医疗器械、83种体外诊断试剂以及三种医疗机器人。目标项目涵盖人工智能独立软件医疗器械、机器人手术设备、体外诊断试剂和动力外骨骼等领域。
相关推荐

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30

瑞典隆德大学开发ProtAIDe-Dx模型,提升神经退行性疾病诊断
2026-04-30
新加坡HistoIndex在美新增肝病学和胃肠病学中心
2026-04-30

美国介入放射学集团与泌尿外科集团签署执业合作
2026-04-30

美国放射学AI企业Azra收购Thynk Health
2026-04-30
