Senseonics一年期持续血糖监测系统Eversense 365获CE认证
2026-02-01 09:43
收藏
医疗设备公司Senseonics近日为其Eversense 365持续血糖监测系统获得CE标志。该设备采用植入皮下的设计,可连续使用一年,与雅培和德康等公司推出的需定期更换的贴片式产品形成区别。Senseonics曾在2017年为该系统的早期版本取得CE认证,并于2018年获得美国食品药品监督管理局批准。

此前推出的早期版本对市场影响有限。Senseonics基于对长效产品市场潜力的判断,开发了Eversense 365持续血糖监测系统,并在2024年取得FDA许可。公司预计2025年销售额将达到3520万美元,较2024年增长56%。
尽管在持续血糖监测领域,德康预计2025年销售额为47亿美元,Eversense 365目前规模较小,但它正推动Senseonics业务增长。公司预测2026年销售额约为6000万美元,这一增长与其从Ascensia收回商业化控制权的策略相关。
终止与Ascensia的合作后,Senseonics于2026年初接管了美国市场业务。欧洲地区的移交需要更长时间。公司首席财务官Rick Sullivan在11月财报电话会议中表示,将在2026年上半年从Ascensia转移负责持续血糖监测的员工,并组建自有销售团队。
Senseonics原计划与Ascensia在2025年下半年推出Eversense 365持续血糖监测系统。随着移交工作推进,公司决定将产品发布时间调整至2026年。Sullivan指出:“我们决定等待建立自身实体并雇佣代表,以确保产品按预期方式推出。这将在上半年进行。在此之前,欧洲市场将保持平稳,之后我们期待看到类似美国以外地区的增长态势。”
相关推荐
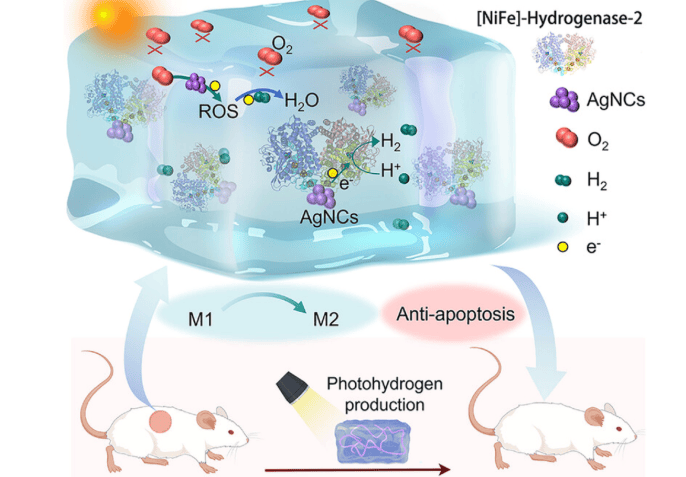
中国南开大学研发光驱动氢化酶系统加速糖尿病伤口愈合
2026-05-05

韩国首尔圣母医院设立听力康复与平衡中心
2026-05-05

美国Ballad Health获机器人手术认证,并在田纳西州投资1500万美元
2026-05-05

意大利Cardioline收购巴西Cardios扩大全球远程心电诊断能力
2026-05-05

澳大利亚EnGeneIC复发性多形性胶质母细胞瘤试验完成首例患者给药
2026-05-05

美国克利夫兰诊所联手Luminai以人工智能医院模式优化运营
2026-05-05

英国SynaptixBio推动语音分析作为神经退行性疾病临床标志
2026-05-05

日本奥林巴斯获EndoRobotics机器人辅助技术全球经销权
2026-05-05

美国TimelyCare通过收购AI平台强化虚拟护理服务
2026-05-05

美国CVRx启动BENEFIT-HF试验首例心力衰竭患者入组
2026-05-05
