信达生物IBI3003获美国FDA快速通道资格
2026-01-27 11:15
收藏
1月27日,信达生物制药集团对外宣布,其自主研发的抗GPRC5D/BCMA/CD3三特异性抗体IBI3003,成功获得美国食品和药物监督管理局(FDA)授予的快速通道资格(Fast Track Designation, FTD)。这一认定旨在加速针对严重疾病且具有未满足医疗需求的新药开发及审评进程。

信达生物研发IBI3003此次拟定的适应症为复发或难治性多发性骨髓瘤(R/R MM),具体针对的是那些已经接受过含一种蛋白酶体抑制剂(PI)、一种免疫调节药物(IMiD)及一种抗CD38单抗的至少四线治疗的患者群体。多发性骨髓瘤作为一种血液系统恶性肿瘤,其复发和难治性病例的治疗一直是临床上的难题。IBI3003通过同时靶向GPRC5D、BCMA和CD3三个靶点,有望为这类患者提供新的治疗选择。
获得FDA快速通道资格,意味着IBI3003在后续的开发过程中将享受与FDA更为紧密的沟通与协作,包括更频繁的会议讨论、更及时的审评反馈等,从而加速其从临床试验到上市应用的进程。信达生物表示,将继续推进IBI3003的临床研究,以期早日为多发性骨髓瘤患者带来创新的治疗方案。
相关推荐

美国LightForce推出患者专用3D打印金属托槽
2026-05-01
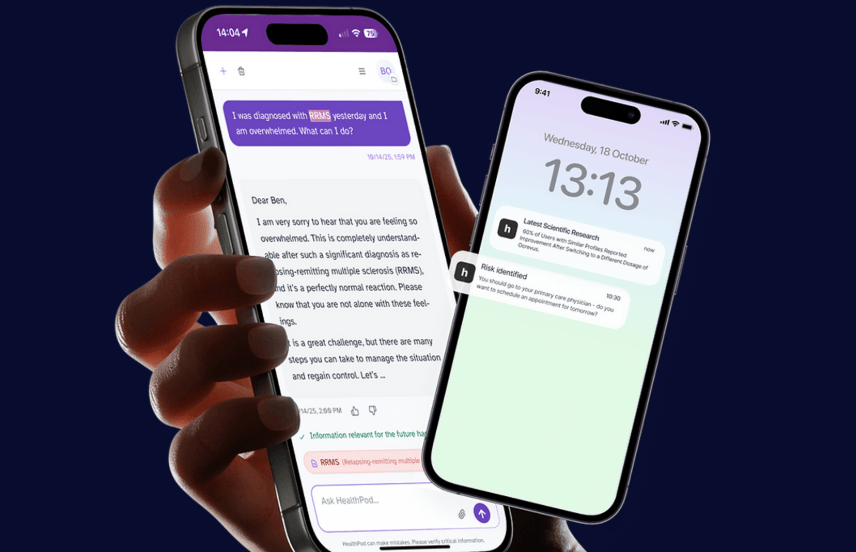
dehaze获320万欧元种子轮融资,用于AI慢性病检测
2026-05-01

诺诚健华研发抑制剂奥布替尼SLE III期临床首例给药
2026-05-01

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
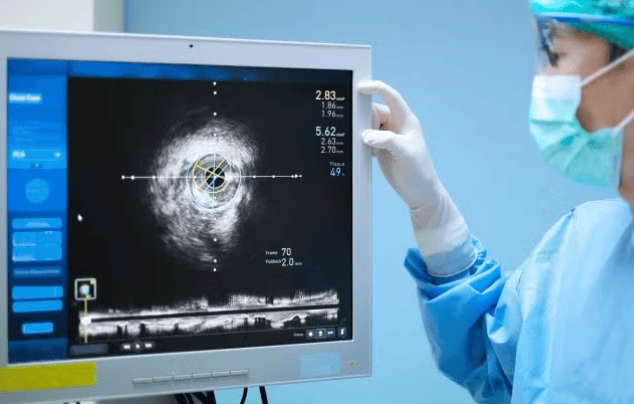
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30

瑞典隆德大学开发ProtAIDe-Dx模型,提升神经退行性疾病诊断
2026-04-30
