BD的乳腺活检系统获FDA批准,预计2026年推向市场
2026-01-16 12:02
收藏
近日,Becton,Dickinson and Company(BD)宣布其研发的EnCor Encompass乳腺活检及组织切除系统已成功获得美国食品药品监督管理局(FDA)的510(k)许可。这一创新性的多模式乳腺活检系统,将为临床医生在乳腺疾病诊断领域提供更为灵活和精准的工具。
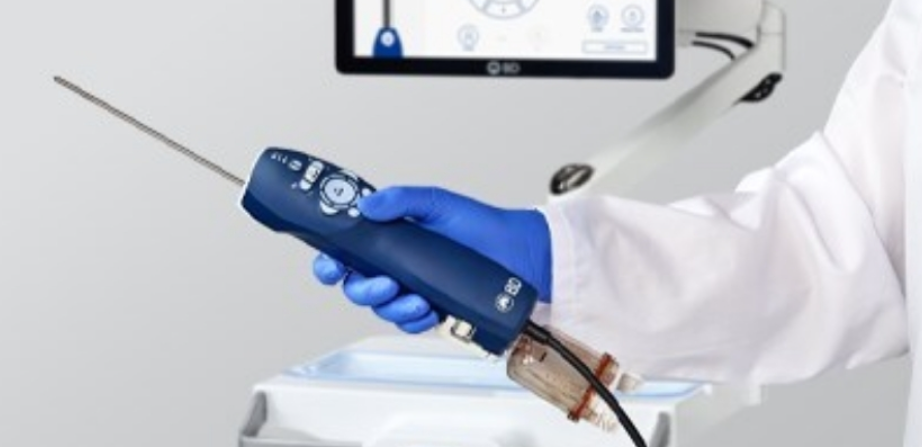
EnCor Encompass系统在设计上充分考虑了临床需求,集成了高低真空强度调节、可变样品缺口以及360度全方位采样能力,确保能够覆盖乳房各个部位的病灶。同时,系统还配备了回声切割导管和发光样本容器,大大增强了操作过程中的可视化效果,提高了活检的准确性。临床医生可以根据不同病灶的类型和位置,灵活选择12G、10G或7G的探头,进一步提升活检的效率和精准度。
BD介入-周围干预肿瘤平台副总裁兼总经理Stacie Watson表示:“EnCor Encompass活检系统获得FDA的批准,是我们对乳腺健康领域临床医生和患者需求持续关注的体现。这一多模式平台通过集成多种先进功能,旨在提升临床医生的操作信心,同时优化患者的诊疗体验。”
加州大学戴维斯分校乳腺放射科主任Shadi Aminollama-Shakeri医学博士也给予了高度评价:“EnCor Encompass系统将多模态能力与增强控制功能完美结合于单一平台,支持程序内的个性化定制,有助于简化活检流程,为患者提供更加高效、安全的诊疗服务。”
据悉,FDA批准的EnCor Encompass系统预计将于2026年初正式进入市场。
相关推荐
加拿大圣迈克尔医院获2.04亿加元投资
2026-06-02

美国SHINE Technologies Ilumira Lu-177获欧盟集中上市许可
2026-06-02

刚果(金)疫情 CEPI 投超6千万美元加速本迪布焦埃博拉疫苗
2026-06-02
丹麦诺和诺德Wegovy口服药获欧洲积极评审,计划推进西班牙上市
2026-06-02
英国研究显示基因检测可让超5000乳腺癌患者免于化疗
2026-06-02

美国Rialtic与Exponential AI宣布合并
2026-06-02

英国NHS数据共享法案预计年减2万急诊并省2000万英镑
2026-06-02

孟加拉国卫生部长称政府已全面准备应对登革热
2026-06-02

美国南卡罗来纳州基金资助农村健康科技初创企业
2026-06-02

中国2026年第三届北京医师协会核医学专科医师分会学术年会召开
2026-06-02