日本中外药厂推进Tecentriq新适应症监管申请
2026-01-29 13:47
收藏
日本中外药厂今日宣布,已正式向厚生劳动省提交了抗癌药物Tecentriq(阿替唑珠单抗)840毫克静脉输注的监管申请,期望将其作为MRD阳性膀胱癌(MIBC)辅助治疗的额外适应症获批使用。此次申请中外药厂在癌症治疗领域又迈出了重要一步,特别是针对那些复发风险较高的特定患者群体。

中外集团总裁兼首席执行官奥田修博士表示:“肌肉侵袭性膀胱癌手术后复发率较高,根据每位患者个体风险优化辅助治疗显得尤为重要。Tecentriq为通过血液检测被识别为高复发风险的患者提供了一种新的辅助治疗选择。中外药厂一直致力于推进癌症护理的个性化,确保每位患者都能获得最适合其病情的治疗方案。”
该监管申请基于全球三期临床IMvigor011研究的结果。该研究评估了Tecentriq单药或安慰剂作为辅助治疗在ctDNA MRD阳性MIBC患者中的疗效和安全性。数据显示,主要终点无病生存期和主要次要终点总体生存期均得到显著改善,且Tecentriq的安全性表现与之前研究中的成熟安全性特征一致。
相关推荐

美国LightForce推出患者专用3D打印金属托槽
2026-05-01
dehaze获320万欧元种子轮融资,用于AI慢性病检测
2026-05-01

诺诚健华研发抑制剂奥布替尼SLE III期临床首例给药
2026-05-01

中国发布首个阿尔法核素医学团体标准
2026-04-30

美国Humbear Media推出人工智能成瘾治疗营销方案
2026-04-30

美国医疗编码平台Arintra推出文档改进功能
2026-04-30
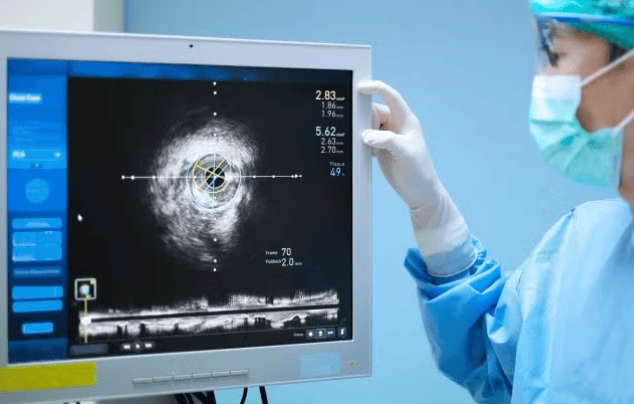
美国雅培Ultreon 3.0成像平台获FDA批准和CE标志
2026-04-30
中国和黄医药Syk抑制剂上市申请获中国国家药监局受理
2026-04-30

英国EnteroBiotix获1900万英镑启动便秘型肠易激综合征2b期试验
2026-04-30

瑞典隆德大学开发ProtAIDe-Dx模型,提升神经退行性疾病诊断
2026-04-30
