威尔康奈尔医学院的研究人员近期在《细胞·微生物与宿主》杂志发表了一项新研究,揭示了肠道细菌如何影响饮食中的天冬酰胺氨基酸,从而在促进肿瘤生长或激活免疫细胞对抗癌症之间起到关键作用。这项发现将肠道微生物组——由数万亿肠道内微生物构成——定位为影响癌症发展及免疫疗法反应的重要因素。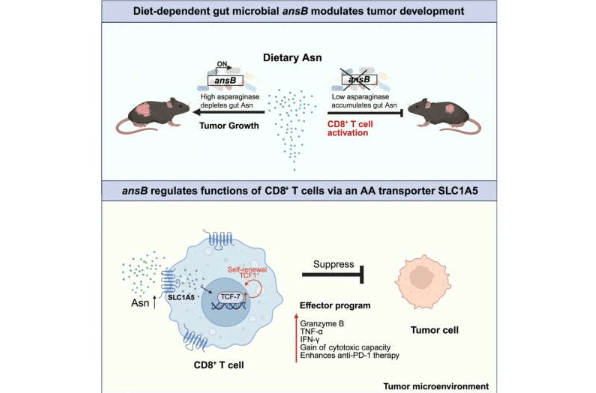
该研究团队通过携带人类肠道微生物群的小鼠模型证实,特定细菌能够消耗氨基酸并干预肿瘤进程。研究重点关注了天冬酰胺,这是一种参与蛋白质合成、维持细胞存活的氨基酸,对肿瘤微环境中的癌细胞和攻击癌细胞的CD8⁺ T免疫细胞都至关重要。
研究人员与一种常见肠道细菌——卵形拟杆菌合作,该菌携带一个名为bo‑ansB的基因,可编码分解天冬酰胺的酶。实验显示,当该基因存在时,细菌在肠道内消耗更多天冬酰胺,导致进入血液并输送至肿瘤的氨基酸减少;基因敲除后,更多天冬酰胺进入循环系统,为肿瘤和免疫细胞提供营养。
在结直肠癌小鼠模型中,高天冬酰胺饮食下,携带bo‑ansB基因的细菌促进了肿瘤生长;而在bo‑ansB缺失的情况下,相同饮食使更多天冬酰胺被CD8⁺ T细胞摄取,促使这些免疫细胞进入“干细胞样”状态,增强抗肿瘤免疫反应。缺乏足够天冬酰胺则削弱了CD8⁺ T细胞的抑癌效果。
进一步研究发现,当bo‑ansB被移除、肿瘤微环境中天冬酰胺水平升高时,CD8⁺ T细胞表面表达更多的SLC1A5蛋白转运体,这对维持干细胞样状态和抗肿瘤活性具有重要意义。阻断SLC1A5则消除了高天冬酰胺带来的免疫增强效果。
该研究的共同负责人、威尔康奈尔大学免疫学副教授郭春俊博士表示:“我们的研究表明,必须关注饮食、肠道微生物群和肿瘤浸润免疫细胞之间的相互作用对癌症生长及治疗反应的影响。这一调控层面不容忽视。”
研究团队指出,未来癌症治疗可能结合免疫疗法、个性化饮食及微生物组干预策略——例如设计益生菌、改造肠道细菌或定制饮食方案,以精细调节氨基酸可用性,优化免疫反应。
共同作者Nicholas Collins博士补充:“饮食对免疫系统的影响可能因个体微生物群差异而不同。我们的目标是实现个性化治疗,通过定制饮食与微生物群协同作用,增强机体抗癌能力。”
这项研究为通过调控肠道微生物组和饮食干预来改善癌症治疗效果提供了新思路。