Celosia Therapeutics启动治疗肌萎缩侧索硬化症的1b期临床试验
2026-03-24 11:27
收藏
澳大利亚生物技术公司Celosia Therapeutics宣布,其1b期KOANEWA试验已完成首例参与者给药。该试验评估CTx1000,这是一种针对肌萎缩侧索硬化症患者中TDP-43蛋白病理形式的在研基因药物。研究正在澳大利亚悉尼的麦考瑞大学医院神经内科进行。肌萎缩侧索硬化症是一种进行性且最终致命的神经退行性疾病,当前治疗选择有限。

Celosia Therapeutics首席执行官Kathryn Sunn博士表示:“ALS是一种进行性且最终致命的神经退行性疾病,治疗选择有限。KOANEWA研究中给药的启动是Celosia的重要里程碑,最重要的是,对于ALS社群来说也是如此。治疗首例患者标志着这种基因药物的临床评估开始,并代表着朝着为ALS患者提供潜在疾病修饰疗法迈出的有意义一步。”
CTx1000旨在清除病理性的TDP-43蛋白,这是肌萎缩侧索硬化症的核心驱动因素。KOANEWA是一项首次人体、开放标签的1b期临床试验,旨在评估单次给药CTx1000在ALS参与者中的安全性和耐受性。除了安全性结果外,该研究还将分析生物标志物和临床指标作为次要探索性疗效终点。
Celosia首席医疗官兼麦考瑞大学痴呆症研究中心主任Lars Ittner教授表示:“这项研究是我们研究计划的重要里程碑,将一种新颖的疾病修饰治疗策略推进到临床,首次直接靶向ALS的基本疾病机制——TDP-43的病理积累。在ALS患者中评估CTx1000将使我们能够评估这种方法的安全性,同时探索其治疗性地解决疾病关键驱动因素的潜力。”该研究为肌萎缩侧索硬化症的治疗探索提供了新的研究方向。
相关推荐

西班牙Aemps更新医疗器械监控文件推动数字化
2026-05-08

英国研究揭示起搏器后心室功能障碍关键因素
2026-05-08
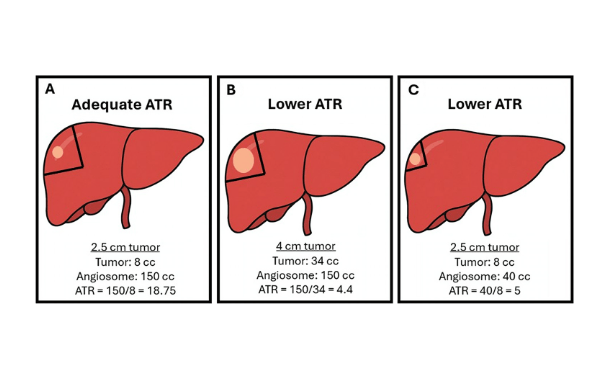
美国放射节段切除术优化参数可提高肝细胞癌完全病理坏死率
2026-05-08
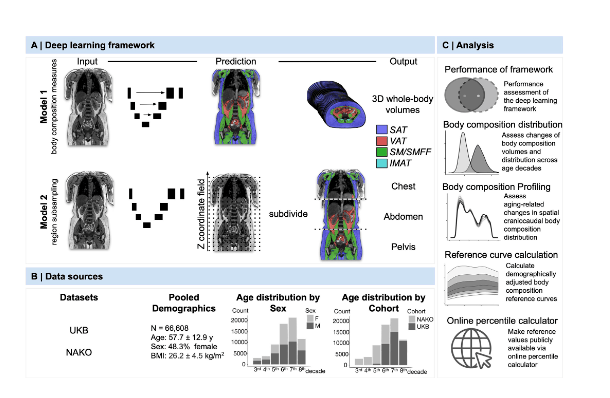
英国与德国超6.6万人全身MRI数据,研究发布身体成分参考曲线
2026-05-08

美国医院协会与西健康研究所合作启动技术推广加速器项目
2026-05-08

马来西亚IHH医疗在新加坡部署Oracle Fusion云统一医疗系统
2026-05-08

澳大利亚TGA批准PEDMARQSI用于预防儿童顺铂相关听力损失
2026-05-08

瑞士Oculis宣布Privosegtor获FDA特殊方案评估协议
2026-05-08

西班牙卫生部批准Roche Columvi新适应症,用于弥漫性大B细胞淋巴瘤
2026-05-08

中国宏碁智医联合New Eye Inc.在泰国普吉府推进智慧医疗生态
2026-05-08
