韩美制药先天性高胰岛素血症药物获FDA突破性疗法认定
2026-02-06 10:32
收藏
韩美制药近日宣布,其研发的先天性高胰岛素血症治疗药物efpegerglucagon获得美国食品药品监督管理局突破性疗法认定。该认定旨在为临床数据表明对严重疾病具有显著治疗潜力的药物提供支持,以加速审批进程。

获得突破性疗法认定的药物在开发过程中将得到FDA的重点指导,并具备滚动审评资格,允许分阶段提交数据。这有助于提升药物开发和审批效率。
韩美制药临床开发负责人李汶熙表示:“通过这一认定,我们将与FDA保持密切沟通,高效推进三期临床试验。同时计划充分利用滚动审评的优势。”
Efpegerglucagon此前已获得美国FDA、欧洲药品管理局和韩国食品药品安全部的孤儿药认定。FDA还将其列为罕见儿科疾病治疗药物,欧洲药品管理局也指定其为治疗胰岛素自身免疫综合征的孤儿药,显示该药物具有广泛的应用前景。
先天性高胰岛素血症是一种罕见疾病,患者因胰岛素分泌过多而反复出现严重低血糖。目前尚无FDA批准的专门治疗方法,现有药物仅对特定基因型有效,且可能引起多毛症、体液潴留等副作用,部分患者不得不使用超说明书药物或接受胰腺切除术。
韩美制药正开发全球首个每周给药一次的efpegerglucagon制剂,以克服现有疗法局限。去年公布的全球二期临床试验中期分析显示,该药物安全性和耐受性良好,能显著减少低血糖事件。全球二期试验预计今年下半年公布结果。
韩美制药研发中心主任崔仁英表示:“FDA的突破性疗法认定是对该药物商业化紧迫性和开发潜力的高度认可。我们将全力加速开发,为患者带来新的治疗希望。”
相关推荐

西班牙Aemps更新医疗器械监控文件推动数字化
2026-05-08

英国研究揭示起搏器后心室功能障碍关键因素
2026-05-08
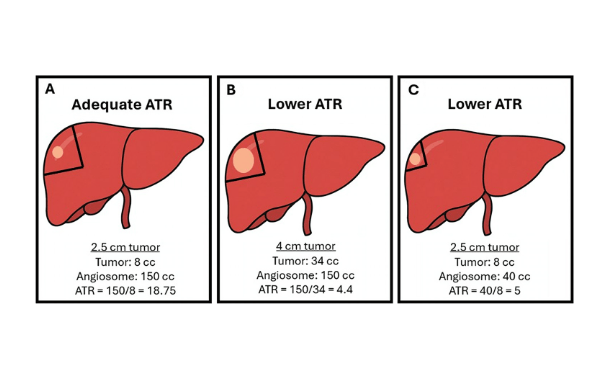
美国放射节段切除术优化参数可提高肝细胞癌完全病理坏死率
2026-05-08
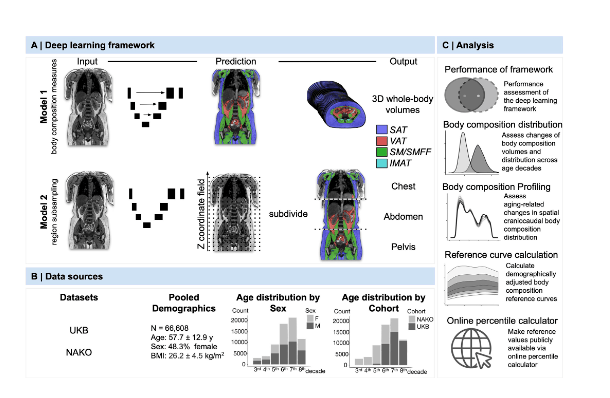
英国与德国超6.6万人全身MRI数据,研究发布身体成分参考曲线
2026-05-08

美国医院协会与西健康研究所合作启动技术推广加速器项目
2026-05-08

马来西亚IHH医疗在新加坡部署Oracle Fusion云统一医疗系统
2026-05-08

澳大利亚TGA批准PEDMARQSI用于预防儿童顺铂相关听力损失
2026-05-08

瑞士Oculis宣布Privosegtor获FDA特殊方案评估协议
2026-05-08

西班牙卫生部批准Roche Columvi新适应症,用于弥漫性大B细胞淋巴瘤
2026-05-08

中国宏碁智医联合New Eye Inc.在泰国普吉府推进智慧医疗生态
2026-05-08
